グリア細胞の増殖プロセスが脳のテント上領域、つまり小脳テント(小脳テント、脳の後頭葉から小脳を隔てる膜)の上に位置する脳の上部部分で発生すると、グリオーシスのテント上病巣が形成されます。
疫学
脳テント上領域の局所性グリオーシスの正確な症例数は算出されておらず、不明です。しかし、脳卒中後では、反応性アストロサイトーシスの病巣が患者の67~98%に認められます。アルツハイマー病では患者の29~100%、パーキンソン病では患者の30~55%に認められます。
臨床統計によれば、てんかん症例の約 26% において、主な神経病理学的異常はびまん性星状膠細胞症であり、これは神経細胞の損傷によって発症するものではありません。
原因 脳実質上部のグリオーシス病巣。
グリオーシスは脳の器質的病変を指し、グリア細胞(脳全体の容積の約半分を占める)の一般的な反応であり、グリア細胞に囲まれた神経細胞(ニューロン)の損傷または死滅に対する反応であると考えられています。[ 1 ] この病変は以下によって引き起こされる可能性があります。
- 頭部外傷の;
- 周産期低酸素症または新生児の出産外傷。
- 脳循環障害中に脳テント上に神経膠症の病巣が生じて血管新生が起こる出血性脳卒中。
- 残存起源の神経膠症のテント上病巣を伴う虚血性脳卒中、すなわち、白質ニューロンの低酸素症および虚血を伴う。
- 小脳卒中;
- コルサコフ症候群の;
- 多発性硬化症における中枢神経系の髄鞘軸索への免疫介在性損傷;
- 血管壁の炎症(血管炎)
- アルツハイマー病;
- パーキンソン病;
- シャルコー神経変性疾患、筋萎縮性側索硬化症。
- 遺伝性ハンチントン病;
- プリオン病、特にクロイツフェルト・ヤコブ病。
- HIV認知症につながる可能性があるエイズ。
- 結核性脳病変の。
高齢者の脳の白質に生じる病理学的変化(ニューロンがグリア細胞に置き換わる)は、小血管アテローム性動脈硬化症の兆候として認識されており、加齢に伴う血管リスク要因と関連しています。
また、結合組織の全身性病変、感染症、脳の悪性腫瘍の場合、血管細小血管症(脳組織内の血液循環障害を伴う小血管壁の病変)を背景にしたテント上神経膠症病巣が発生する可能性もあります。
危険因子
さらに、脳の神経膠症病巣の危険因子は、慢性高血圧、高脂血症および低血糖、長期の脳血液循環障害(脳組織の低酸素症につながる)、長期の新生児仮死(脳組織の低酸素症につながる)、さまざまな遺伝病理および遺伝性疾患、てんかん、脳感染症(脳炎、ウイルス性髄膜炎)、メタボリックシンドロームおよびアルコール依存症と関連している。[ 2 ]
病因
神経生理学者は、神経膠症の発症機序を局所的な脳損傷に対する普遍的な反応、または中枢神経系における一般的な病理学的プロセスとみなし、この反応のメカニズムの不確実性に注目しています。
しかし、脳のグリア細胞は神経細胞とは異なり、年齢に関係なく分裂によって増殖できることは確実に知られています。グリア細胞はニューロンの安定した位置を維持するだけでなく、ニューロンに栄養を与え、ニューロンとそのシナプスを取り囲む細胞外液を調節します。
炎症性サイトカインである IL-1 (インターロイキン-1)、IL-6 (インターロイキン-6)、TNF-α (腫瘍壊死因子アルファ) がグリア細胞 (アストロサイト、ミクログリア細胞、オリゴデンドロサイト) の活性化と増殖を促進する役割を果たすことが明らかになりました。
例えば、脳損傷に対する反応として、アストロサイト(星状グリア細胞)は炎症の化学伝達物質を放出し、好酸球や一部の栄養性血液因子を誘引します。これにより、グリア線維性酸性タンパク質(GFAP)の発現が亢進し、グリア細胞の肥大とアストロサイトの増殖が促進されます。その結果、神経組織の欠損部を埋めるグリア瘢痕が形成されます。同時に、星状細胞は損傷した軸索の再生を阻害します。
脳に常在する食細胞であるミクログリアは、炎症性サイトカインや成長因子によっても活性化され、マクロファージに分化し、脱髄疾患や神経変性疾患において免疫反応を引き起こす可能性があり、ニューロンやその軸索への損傷にも反応します。
さらに、脳卒中における神経膠症のプロセスは、脳の毛細血管の損傷と血液脳関門の完全性の一時的な破壊によって始まる可能性がある。[ 3 ]
症状 脳実質上部のグリオーシス病巣。
専門家は、局所的または単一の神経膠症のテント上病巣(1か所でのかなり大規模な神経膠細胞の過剰増殖の形態)、少数の病巣(2つまたは3つ以下)、および複数の神経膠症のテント上病巣(3つ以上)、および拡散性または多巣性のテント上病巣を区別します。
したがって、テント上グリオーシス病巣の一般的な症状と初期兆候は、病巣が単一か複数かによって異なりますが、主にその特定の局在によって決定されます。場合によっては、このような病巣は神経学的に何ら症状を示さないこともあります。
テント上構造は、大脳基底核と視床を含む大脳半球、後頭葉(視覚と眼球運動機能を制御)、頭頂葉(身体的感覚の知覚と解釈を可能にする)、前頭葉(論理、知性、個人の思考と言語の発達を担う)、および側頭葉(短期記憶と言語を担う)です。
したがって、グリア細胞による局所ニューロンの置換の臨床像には、頭痛やめまい、急激な血圧変動、運動機能障害(歩行の変化、運動失調、麻痺、体のバランス維持の困難、発作)、感覚障害、視覚、聴覚または言語の問題、注意力、記憶力および認知機能の低下、ならびに認知症の症状である行動障害が含まれる可能性がある。
血管起源のテント上神経膠症病巣のほとんどの症例では、循環不全性脳症に特徴的な症状がみられる。[ 4 ]
合併症とその結果
テント上領域の局所性神経膠症の主な悪影響は脳機能の障害であり、認知障害、認知症、歩行障害、幻覚、うつ病などの症状として現れることがあります。
局所神経膠症の合併症により、患者の完全な障害のリスクが高まります。
診断 脳実質上部のグリオーシス病巣。
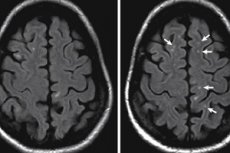
機器による診断のみ -脳の磁気共鳴画像法(MRI)を使用。グリオーシスのテント上病巣を検出できます。
グリオーシスの単一のテント上病巣を視覚化したMR画像では、異なる形状の非常に顕著な明るい領域の形で示され、それはテント上病巣に属する脳構造の異なる領域に局在することができる。[ 5 ]
差動診断
鑑別診断は、星細胞腫、頭蓋咽頭腫、血管芽腫、上衣腫、脳軟化症と合わせて行われます。
処理 脳実質上部のグリオーシス病巣。
治療は、脳実質内の神経膠症の病巣(除去できない)を対象とするのではなく、脳への正常な血液供給を確保し、栄養神経細胞とそこで起こる代謝プロセスを改善し、低酸素症と酸化ストレスに対する抵抗力を高めることを目的としていることに留意する必要があります。
カビント(ビンポセチン)とシンナリジンは、脳血流の正常化に貢献します。また、脳神経細胞の代謝は、セレブロリジン、ピラセタム、フェザム(ピラセタム+シンナリジン)、セレトン(セレプロ)、セラクソン、ゴパンテン酸カルシウムといった向知性薬の使用によって刺激されます。
リポ酸製剤は抗酸化剤として処方されることがあります。
防止
一般的な予防には、健康的なライフスタイルの原則としてよく知られています。しかし、脳のテント上領域にグリオーシス病巣が出現する疾患を考慮すると、動脈硬化症や脳卒中をはじめとするこれらの病態を予防するための予防措置を講じる必要があります。
アルツハイマー病を予防するための推奨事項もあります。
予測
神経膠症のテント上病巣の局在と分布、およびその病因と症状の強度は、中枢神経系の新興疾患全体の予後に直接影響を及ぼし、患者の生活の質に影響を及ぼします。


