記事の医療専門家
新しい出版物
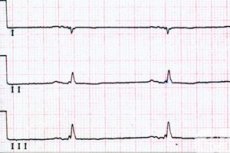
原因 洞性徐脈
心拍数の低下という症状が現れるからといって、必ずしも病気を意味するわけではありません。例えば、睡眠中の心拍数は覚醒時よりも低くなります。そのため、生理的な洞性徐脈と症状のある(病的な)洞性徐脈を区別する必要があります。そして、ほとんどの場合、医師は原因を特定することができます。
したがって、低体温(すべての代謝プロセスの減速を伴う体の低体温)中の心拍数の低下は、高齢の男性と女性に気付かれない洞性徐脈(加齢による心臓の変化の結果)と同様に、病状とは見なされません。
スポーツ選手における洞性徐脈は生理的なものであり、高頻度で変動する高音を伴います。運動負荷の増加により心拍数が減少し、心室容積と心圧が上昇するため、スポーツ選手のほぼ半数は洞性徐脈と左室肥大を同時に呈しています。詳細については、「スポーツ心臓」をご覧ください。
生理学的には、妊娠中の洞性徐脈も発生します。妊娠前半は中毒性初期症状である頻繁な嘔吐によって発生し、後期には子宮が下大静脈に機械的な圧力をかけ始めることで発生します。しかし、貧血のために、妊婦は洞性頻脈を経験することもあります。
一方、心拍数の持続的な低下は、鬱血性心筋症および肥大型心筋症、感染性心筋炎および心内膜炎、心筋梗塞後症状、甲状腺機能低下症(甲状腺ホルモンの欠乏)、血液中のカリウムおよび/またはマグネシウムの欠乏(電解質不均衡につながる)、動脈性低血圧および自律神経性血管性ジストニア、副腎または下垂体の障害、頭蓋内圧の上昇、脳に局在する炎症(ライム病など)、腫瘍など、さまざまな病態および疾患の症状である可能性があります。
洞性徐脈の主な原因は、心臓伝導系の障害であり、その中で主要なペースメーカーである右心房の洞結節(洞房結節)が重要な役割を果たします。そして、洞結節の機能における病理学的異常の組み合わせが心拍数の低下につながる場合、洞不全症候群と呼ばれます。
しかしながら、洞性徐脈における伝導障害は、房室結節の障害、すなわち房室ブロック(AVブロック)とも関連しており、その臨床的意義は洞房結節の弱化を凌駕します。また、AV結節より下における刺激伝導障害は、レネグレット症候群(伝導系の特発性線維化および石灰化)によって引き起こされます。
危険因子
心拍数が持続的に低下する危険因子には、心臓に合併症を引き起こす感染症や自己免疫疾患、あらゆる病因による出血や低酸素症、自律神経反射亢進、老齢、長期の臥床、食欲不振や「飢餓ダイエット」、有毒物質への曝露(中毒)、喫煙、アルコール乱用、ストレスなどがあります。
重要な医原性要因としては、βアドレナリン受容体またはカルシウムチャネルを遮断する抗不整脈薬(アミオダロン、ベラパミル、プロプラノロールなど)、強心配糖体(ジギタリス群)、三環系抗うつ薬およびフェノチアジン群の神経遮断薬、鎮静剤(バロコルジンおよびその類似体を含む)の長期使用が挙げられます。
ペースメーカーの弱化および徐脈の発生の危険因子としては、心筋虚血、心筋梗塞(右心房または心室中隔領域の瘢痕を伴う)、洞結節の心筋細胞の損傷を伴う心筋の局所的およびびまん性の変性変化(硬化、石灰化)などがあります。
病因
心臓専門医が指摘するように、副交感神経緊張亢進による洞性徐脈の病因は、洞房結節領域を支配する迷走神経とその枝の過剰興奮にあります。
洞機能不全は、いくつかの要因によって引き起こされる可能性があります。第一に、洞への十分な血液供給が阻害され、洞を構成する細胞の栄養状態が低下すると、心拍数が低下します。第二に、ペースメーカーの自動機能が部分的に「オフ」になり、低速で作動します。その結果、心筋細胞(ペースメーカーニューロン)の洞脱分極間隔が長くなり、洞性徐脈と洞性不整脈、または洞性徐脈と上室性頻脈と呼ばれる状態につながる可能性があります。このような状態はフレデリック症候群と呼ばれます。
洞結節が弱い場合、ヒス束から拍動が発生し始めますが、予想よりも早く発生し、心房を迂回して心室の筋線維を交互に収縮させます。このような状況では、洞性徐脈や期外収縮と診断されることがあります。
第 2 度および第 3 度の AV ブロックにより、洞細胞から心房の心筋へ、または心房から心室へ、刺激が自由に伝達されないため、刺激の伝達自体が妨げられる可能性があります。
また、房室結節と房室束(ヒス束)の間で脈動が遅延することもあります。その場合、房室徐脈と定義する方が正確でしょう。詳しくは「心臓の伝導系」をご覧ください。脈動の通過が部分的に途絶し、心拍数が低下し、右心室圧が上昇する場合は、右ヒス束の不完全ブロックと洞性徐脈が考えられます。洞性徐脈は、僧帽弁の狭窄や逸脱、虚血、先天性心疾患、急性心筋梗塞、そしてジギタリス製剤(強心配糖体)の副作用として現れることがあります。
心室血行動態の障害に関連する心臓欠陥の場合、心室収縮期に心室中の圧力が上昇し、心拍数が低下し、収縮期負荷を伴う洞性徐脈が観察されます。
甲状腺ホルモンが心拍リズムに及ぼす影響を説明する専門家は、甲状腺機能低下症患者におけるトリヨードサイロニンとチロキシンの合成不足により、水塩代謝が阻害されるだけでなく、交感神経副腎系のクロマチン組織内受容体の興奮性も低下することを強調しています。その結果、細胞がカルシウムイオンを捕捉する量が大幅に減少し、心拍数、心拍出量、収縮期血圧が低下します。
症状 洞性徐脈
前述の通り、ICD-10では洞性徐脈は症状、徴候、および正常範囲からの逸脱の分類においてクラスXVIIIに分類されています。洞性徐脈の最初の兆候は、心拍数が毎分58~55回まで低下することです。この低下は全く感じられない場合もあり、これは軽度の洞性徐脈です。
しかし、心拍数が低下すると、洞性徐脈は心臓機能および全身の血行動態の障害に関連する特定の症状を引き起こす可能性があります。症状の強さと範囲は、1分間の心収縮回数の減少の程度によって異なります。55~40回は中等度の洞性徐脈、40回未満は重度の洞性徐脈です。
したがって、原因を問わず洞性徐脈に伴う非特異的な症状には、急速な疲労、全身の脱力感、めまい(失神することもある)、冷や汗、軽い吐き気、呼吸困難、胸部の不快感などがあります。
重度の洞性徐脈(心拍数が毎分30回以下に低下する状態)は、緊急末期状態(特に、外傷による循環血液量の著しい減少、重度の中毒、心臓性ショック、甲状腺機能低下性昏睡など)に分類されます。この症状は、チアノーゼ、四肢冷感、激しいめまい、瞳孔収縮、けいれん、血圧低下、意識消失、呼吸停止などの症状として現れます。
小児および青年における洞性徐脈
年少の子供では、身体の恒常性を保つ主な生理学的プロセス(体温、血圧、心拍数など)が自律神経系(ANS)の交感神経系によって制御されているため、心臓の鼓動は大人よりも速くなります。
新生児における洞性徐脈は、心拍数が1分間に100回未満(正常は120~160回程度)と定義され、分娩時の窒息を伴う。また、部分的な房室ブロックを伴う持続性徐脈は、先天性全身性エリテマトーデスまたは遺伝性QT延長症候群の兆候と考えられている。
また、小児の洞性徐脈は、心臓手術後に発症する洞不全症候群や先天性右心室肥大の結果である場合もあります。
心臓専門医が十代の若者に検出する洞性徐脈は、洞結節の同様の弱さにより発症する可能性もありますが、ほとんどの場合、思春期に特徴的な自律神経系障害の症状(ホルモンの変化による)であることが判明します。
思春期の若者の中には、この症状に交感神経優位の症状を伴う者もいれば、迷走神経緊張の兆候が認められる者もいます。迷走神経緊張とは、自律神経系の副交感神経系によって生理機能が主に「制御」されている状態です。これは遺伝的に決定され、副交感神経性過緊張と呼ばれ、発汗の増加、動脈性低血圧、洞性徐脈の発作として現れます。
自律神経系の両方の部分が同じように興奮している場合、これはアンフォトニアであり、さまざまな状況で徐脈、洞性徐脈性不整脈、発作性頻脈(つまり発作性)が交互に発生する可能性があります。
フォーム
この心拍リズム障害には単一の体系化はなく、さまざまな情報源によって洞性徐脈のタイプが次のように定義されています:生理的、症候性(病的または相対的)、絶対的、中枢性、器質性(心臓内、すなわち主要な器質性心疾患による)、心臓外性(心疾患に関連しない)、変性、毒性、特発性(病因不明)。
垂直洞性徐脈は、生理学的に心臓の電気軸(EOS)の位置変化を伴うものと区別されます。さらに、心電図では、EOSの左偏位(左室肥大の特徴)または右偏位(右室肥大の可能性あり)が明らかになることがあります。これらの変化は無症状の場合もあれば、非特異的な症状として現れる場合もあります。
合併症とその結果
急性洞性徐脈がいかに危険であるかはすでにご存じのとおりですが、それほど顕著ではない症状、毒性、または特発性の心収縮回数の減少も、結果や合併症を引き起こす可能性があります。
その中には、心臓の個々の構造への血液供給不足による疼痛症候群(狭心症)の発症、機能性心臓障害(心不全)、血栓形成の増加、脳卒中、心臓発作、モルガニ・アダムス・ストークス症候群の発症などがあります。
診断 洞性徐脈
診断には、脈拍、血圧の測定、聴診器による聴診、血液検査(生化学検査、甲状腺ホルモンおよび電解質レベル、リウマチ複合体)が含まれます。
病歴には、患者がこれまでに患ったすべての病気と服用した薬に関する情報が含まれている必要があります。
機器による診断は、12 誘導心電図(および 24 時間ホルター心電図)、心エコー検査、必要に応じて胸部の超音波検査または MRI を使用して、重要な役割を果たします。
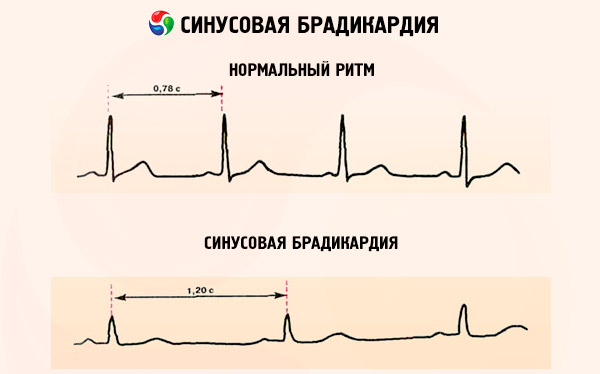
洞性徐脈は、心電図上では心拍数の低下(R波の間隔が長くなる)、洞調律の存在(P波は常に正で、各心室複合体(QRS)の前に固定される)、およびQRS複合体の幅の拡大によって確認できます。
ECG 上のヒス束内またはその下で発生した刺激は、心拍数が 20 ~ 40 bpm の広い QRS 群を形成します。
何を調べる必要がありますか?
どのように調べる?
差動診断
洞性不整脈、脱分極障害、早期心室再分極症候群などの心律動異常の鑑別診断も、正常時および身体活動時の心電図に基づいて行われます。
徐脈または徐脈性不整脈は、心室による電気刺激の伝達の問題によっても発生する可能性があり、心室内伝導障害は、心虚血および動脈硬化、心内膜炎、またはリウマチによって引き起こされる心臓弁の病変がある患者で検出されます。
詳細については、「心拍リズムおよび伝導障害」の資料をご覧ください。
連絡先
処理 洞性徐脈
欧州心臓病学会の専門家によると、全体的な血行動態に悪影響を及ぼす心拍の遅延に明らかに関連する症状がない限り、ほとんどの人にとって洞性徐脈の治療は必要ありません。
症状がある場合、どのような治療を、どのように行うべきでしょうか?心拍数低下の原因とそれに伴う症状によって異なります。洞性徐脈が甲状腺機能低下症によって引き起こされている場合は、ホルモン補充療法(レボチロキシン)が適応となります。感染性心筋炎には抗生物質の使用が必要であり、カリウムとマグネシウムの欠乏の場合は、カリウムとマグネシウムを含む錠剤(パナンガン、クデサン、カリノール、オロチン酸カリウムなど)が処方されます。
重篤な臨床症状や重症房室ブロックを伴う洞房結節機能不全には治療が必要であり、これはもっぱら永久ペースメーカーの植え込みによる外科的治療である。
その他の場合、心拍数を増加させるために、正の変時作用を持つ薬剤が処方されることがあります。これは、M-コリン受容体を遮断する薬剤とβ-アドレナリン受容体を刺激する薬剤によってもたらされます。これらの薬剤には、アトロピン、イサドリン(イソプレナリン)、臭化イプラトロピウム(他の商品名:イトロプ、アトロベント、バゴス、ノルモセクレトール)、オルシプレナリン(アストモペント、アルペント、アロテック)、エフェドリン、エピネフリン(アドレナリン)、ノルエピネフリンなどがあります。
臭化イプラトロピウム錠(0.01g)および注射液は医師の処方のみ可能であり、医師は投与量(標準:1日2回0.5~1錠)を決定します。この薬剤は、排尿、発汗、排便機能、排便を阻害し、口腔粘膜を乾燥させ、食欲を減退させる可能性があります。前立腺肥大症、緑内障、腸狭窄症、妊娠(妊娠初期)には禁忌です。
アテローム性動脈硬化症の既往歴がない場合は、オルシプレナリン0.05%溶液錠(20mg)を使用できます。この薬は、徐脈性不整脈や強心配糖体服用後の心拍数減少に特に効果的です。投与量と治療期間は主治医が決定します。
重度の洞性徐脈は呼吸停止につながり、さらに心停止に至る場合もあり、アトロピン投与や心臓刺激による緊急治療が必要となります。
予測
予後は多くの要因に左右されます。重度の洞性徐脈(40 bpm未満)では、「遅い」心臓が体に必要な量の血液を供給できなくなります。これは悪影響を及ぼし、生命を脅かす可能性があります。
甲状腺機能低下症の患者は、甲状腺ホルモンによる治療で徐脈などの症状を緩和できるため、予後は良好です。
かつては、第3度房室ブロックの患者の予後は不良で、診断後1年以内に50%の患者が死亡していました。しかし、永久ペースメーカーの植え込みにより、状況は劇的に改善されました。
兵役とスポーツ
洞性徐脈は、重度の心不全を伴う場合、軍隊への入隊は不可能です。無症状の軽度または中等度の徐脈の場合、徴兵された兵士の運命は医療委員会によって決定され、軍務に「限定的に適格」となるかどうかが判断されます。
洞性徐脈がある場合でもスポーツをすることは可能かどうかという質問にも、徐脈の原因を検査・解明した上で、心臓専門医が答えるべきです。しかし、この心拍リズム障害がある場合でも、健康状態を著しく悪化させることなく適度な運動を行うことは歓迎されます。



 [
[