原因 子宮癌
子宮内膜がんの発症において特別な位置を占めるのは、子宮内膜の背景状態(腺性増殖、子宮内膜ポリープ)と前がん状態(異型増殖および腺腫症)です。
 [ 9 ]
[ 9 ]
危険因子
リスクグループには、特定の疾患や状態(リスク因子)を患い、悪性腫瘍を発症する可能性が高い女性が含まれます。子宮がんを発症するリスクグループには、以下のようなものがあります。
- 閉経期にあり、生殖管から血性の分泌物が出る女性。
- 50 歳を過ぎても月経機能が継続している女性、特に子宮筋腫のある女性。
- 子宮内膜の過形成(再発性ポリープ症、腺腫症、子宮内膜の腺嚢胞性過形成)を患っているあらゆる年齢の女性。
- 脂肪および炭水化物代謝障害(肥満、糖尿病)および高血圧の女性。
- 無排卵およびエストロゲン過剰症を引き起こすさまざまなホルモン障害を持つ女性(シュタイン・レーベンタール症候群、産後神経内分泌疾患、子宮筋腫、子宮腺筋症、内分泌不妊症)。
子宮内膜がんの発生に寄与するその他の要因:
- エストロゲン補充療法。
- 多嚢胞性卵巣症候群。
- 出産歴なし。
- 初潮が早く、閉経が遅い。
- アルコールの乱用。
症状 子宮癌
- 白帯下(白帯下)。子宮がんの最も初期の兆候です。白帯下はサラサラとした水っぽいおりもので、特に運動後には血が混じることがよくあります。
- 外性器のかゆみ。子宮内膜がん患者では、膣分泌物による刺激により起こることがあります。
- 出血は腫瘍の崩壊の結果として起こる後期症状であり、肉のような「塊」、汚れ、または純血の形での分泌物として現れることがあります。
- 子宮からの排出が遅れると、下肢に放散する痙攣のような痛みが生じます。鈍痛、特に夜間に感じる痛みは、子宮外への進行を示しており、腫瘍浸潤による小骨盤内の神経叢の圧迫によって説明されます。
- 膀胱または直腸への腫瘍の成長により生じる隣接臓器の機能障害。
- これらの患者は肥満(体重減少はまれ)、糖尿病、高血圧を特徴とします。
あなたを悩ましているのは何ですか?
ステージ
現在、臨床診療では、1985 年分類、国際 FIGO 分類、TNM 分類など、子宮癌のいくつかの分類が使用されています。
 [ 18 ]
[ 18 ]
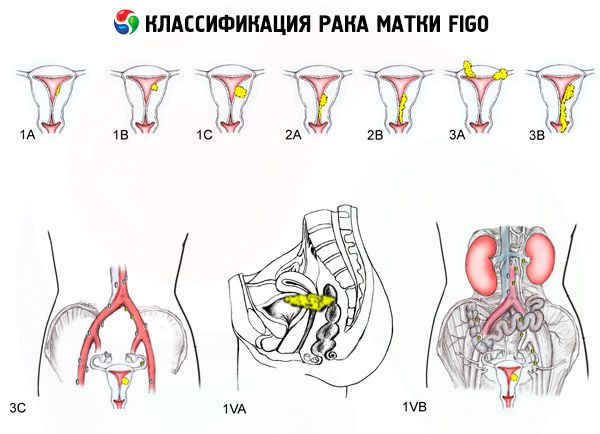
FIGO子宮癌のステージ分類
病変の範囲
- 0 - 子宮内膜前癌(子宮内膜の非典型腺性増殖症)
- 1 - 腫瘍は子宮体部に限局しており、局所転移は検出されない
- 1a - 腫瘍が子宮内膜に限局している
- 1b - 子宮筋層への1cmまでの浸潤
- 2 - 腫瘍が子宮体部および子宮頸部に影響を及ぼし、局所転移は判定されない
- 3 - 腫瘍は子宮を越えて広がっているが、骨盤を越えてはいない
- 3a - 腫瘍が子宮漿膜に浸潤している、および/または子宮付属器および/または骨盤の所属リンパ節に転移がある
- 3b - 腫瘍が骨盤組織に浸潤している、または膣に転移している
- 4 - 腫瘍が骨盤を越えて広がっており、膀胱や直腸に浸潤している
- 4a - 腫瘍が膀胱および/または直腸に浸潤している
- 4b - 局所および領域拡散の程度を問わず、遠隔転移が検出された腫瘍
TNMシステムによる子宮癌の国際分類
- T0 - 原発腫瘍は検出されない
- Tis - 浸潤前癌
- T1 - 腫瘍が子宮体部に限局している
- T1a - 子宮腔の長さが8cm以下
- T1b - 子宮腔の長さが8cmを超える
- T2 - 腫瘍は子宮頸部まで広がっているが、子宮の外には広がっていない
- T3 - 腫瘍は子宮を越えて広がっているが、骨盤内にとどまっている
- T4 - 腫瘍が膀胱や直腸の内壁に広がり、骨盤を越えて広がっている
N - 所属リンパ節
- Nx - 所属リンパ節の状態を評価するためのデータが不十分
- N0 - 所属リンパ節への転移の証拠なし
- N1 - 所属リンパ節転移
M - 遠隔転移
- Mx - 遠隔転移を判定するにはデータが不十分
- M0 - 転移の兆候なし
- M1 - 遠隔転移あり
G - 組織学的分化
- G1 - 高度な分化
- G2 - 平均分化度
- G3-4 - 分化度が低い
フォーム
子宮がんには、限局型とびまん型があります。限局型では、腫瘍はポリープ状に増殖し、子宮の正常な粘膜とは明確に区別されます。びまん型では、がんの浸潤が子宮内膜全体に広がります。腫瘍は子宮底部と卵管角部に最も多く発生します。患者の約80%は様々な分化度の腺がんであり、そのうち8~12%はアデノアカントーマ(良性の扁平上皮細胞分化を伴う腺がん)で、予後は良好です。
予後が悪い、あまり一般的ではない腫瘍には腺性扁平上皮癌があります。腺性扁平上皮癌の扁平上皮細胞成分は扁平上皮癌に似ていますが、分化していない腺性成分が存在するため予後は悪くなります。
扁平上皮癌は、明細胞癌と同様に、子宮頸部の類似の腫瘍と多くの共通点があり、高齢の女性に発生し、攻撃的な経過をたどるのが特徴です。
未分化癌は60歳以上の女性に多く見られ、子宮内膜萎縮を背景に発症します。また、予後は不良です。
子宮内膜がんのまれな形態学的変異の一つに漿液性乳頭がんがあります。形態学的には漿液性卵巣がんと多くの共通点があり、極めて悪性度の高い経過と高い転移の可能性を特徴としています。
診断 子宮癌
婦人科検診。鏡を用いた検診では、子宮頸部の状態と子宮頸管からの分泌物の性質を明らかにし、分泌物を採取して細胞診を行います。膣(直腸膣)検診では、子宮の大きさ、子宮付属器および子宮傍組織の状態に注意を払います。
吸引生検(子宮腔からの吸引細胞診)と子宮腔および子宮頸管からの吸引洗浄液の検査。後者は、吸引生検と診断的掻爬が不可能な閉経後に実施されます。
後円蓋から採取した膣スメアの細胞診。この検査法では42%の症例で陽性結果が得られます。
肯定的な結果の割合は小さいものの、この方法は外来診療で広く使用でき、外傷がなく、腫瘍の進行を刺激しません。
子宮鏡検査下で、子宮腔と子宮頸管を別々に診断的に掻爬する。前癌病変が最も発生しやすい部位、すなわち外子宮口、内子宮口、そして卵管角から擦過検体を採取することが推奨される。
子宮鏡検査。この方法は、掻爬が困難な部位における癌の進行過程を特定し、腫瘍の進行部位と広がりを特定するのに役立ち、治療法の選択やその後の放射線療法の有効性のモニタリングに重要です。
腫瘍マーカー。子宮内膜癌細胞の増殖活性を調べるために、モノクローナル抗体Ki-S2、Ki-S4、KJ-S5を測定することが可能です。
遠隔転移を検出するには、胸部X線検査、超音波検査、腹部臓器および後腹膜リンパ節のコンピューター断層撮影を行うことが推奨されます。
超音波検査。超音波診断の精度は約70%です。場合によっては、癌リンパ節と子宮筋の音響特性が実質的に区別できないこともあります。
コンピュータ断層撮影(CT)。子宮付属器への転移や原発性多発卵巣腫瘍を除外するために行われます。
磁気共鳴画像法(MRI)。子宮内膜がんにおけるMRIは、進行の正確な位置を特定し、ステージIおよびIIをステージIIIおよびIVと区別するだけでなく、子宮筋層への浸潤の深さを特定し、ステージIとその他の段階を区別することを可能にします。MRIは、子宮外での進行の有無を判断する上で、より有益な情報を提供する方法です。
何を調べる必要がありますか?
どのように調べる?
処理 子宮癌
子宮がんの患者の治療法を選択する際には、主に次の 3 つの要素を考慮する必要があります。
- 年齢、患者の全般的な状態、代謝および内分泌障害の重症度。
- 腫瘍の組織学的構造、分化の程度、大きさ、子宮腔内での局在、および腫瘍プロセスの普及率。
- 治療が行われる施設(医師の腫瘍学の研修と外科手術の技術だけでなく、施設の設備も重要です)。
上記の要素を考慮することによってのみ、プロセスを正しく段階的に実行し、適切に処理することができます。
子宮がんの患者の約90%は外科的治療を受けます。通常は子宮および付属器の摘出が行われます。腹腔を開腹した後、骨盤内臓器、腹腔、後腹膜リンパ節の再建術が行われます。さらに、ダグラス窩からスワブを採取し、細胞診を行います。
子宮癌の外科的治療
外科的治療の範囲は、プロセスの段階によって決まります。
ステージ1a:子宮内膜のみが侵されている場合、腫瘍の組織学的構造や分化度に関わらず、子宮付属器を含む子宮の単純摘出術のみで追加治療は不要です。内視鏡手術の登場により、この段階でも子宮内膜の焼灼術(ジアテルモ凝固術)が可能になりました。
ステージ 1b: 表層浸潤、小さな腫瘍の局在、子宮の上部後部での高度分化の場合、付属器とともに子宮の単純摘出が行われます。
子宮筋層の1/2までの浸潤、分化度G2およびG3、腫瘍サイズが大きく、子宮下部に局在している場合は、付属器を含めた子宮摘出術およびリンパ節郭清が適応となります。小骨盤リンパ節に転移がない場合は、術後に膣腔内照射を行います。術後にリンパ節郭清が不可能な場合は、小骨盤への体外照射を行い、総線量45~50Gyを照射します。
ステージ1b-2a G2-G3;2b G1では、子宮付属器を含む摘出術とリンパ節郭清術が行われます。リンパ節転移および腹水中の悪性細胞がなく、浅い浸潤の場合は、術後に膣腔内照射療法を実施します。深達度が高く、腫瘍の分化度が低い場合は、放射線療法を実施します。
ステージ3:最適な手術量は、リンパ節郭清を伴う子宮付属器摘出術とします。卵巣転移が認められた場合は、大網を切除する必要があります。その後、小骨盤への外部照射を行います。傍大動脈リンパ節転移が認められた場合は、切除することが推奨されます。転移性リンパ節を切除できない場合は、この部位への外部照射を行う必要があります。ステージIVでは、可能であれば、手術療法、放射線療法、化学ホルモン療法を用いて、個々の患者に合わせた治療計画に従って治療を行います。
化学療法
このタイプの治療は、主に広範囲にわたるプロセス、自律性腫瘍(ホルモン非依存性)の場合、および病気の再発と転移が検出された場合などに行われます。
現在、子宮がんに対する化学療法は、いくつかの薬剤が十分に有効であっても、その作用期間が通常 8 ~ 9 か月と短いため、緩和療法にとどまっています。
第一世代(シスプラチン)または第二世代(カルボプラチン)のプラチナ誘導体、アドリアマイシン、シクロホスファミド、メトトレキサート、フルオロウラシル、ホスファミドなどの薬剤の組み合わせが使用されます。
最も効果的な薬剤の中には、20%以上の症例で完全および部分的な効果をもたらすものとして、ドキソルビシン(アドリアマイシン、ラストシンなど)、ファルマビシン、第 1 世代および第 2 世代のプラチナ製剤(プラチディアム、シスプラチン、プラチマイト、プラチノール、カルボプラチン)があります。
アドリアマイシン(50 mg/m2 )とシスプラチン(50~60 mg/m2 )を併用すると、最大60%の効果が得られます。
広範囲子宮癌、その再発および転移に対して、タキソールは単剤化学療法および他剤との併用療法のいずれにおいても使用できます。単剤療法では、タキソール175 mg/m²を3週間ごとに3時間かけて点滴します。タキソール(175 mg/m²)、シスプラチン(50 mg/m² )、エピルビシン(70 mg/m² )との併用により、治療効果は著しく向上します。
ホルモン療法
手術までに腫瘍が子宮外に転移している場合、局所的な外科手術や放射線治療では根本的な治療上の問題は解決しません。化学療法とホルモン療法が必要になります。
ホルモン治療では、プロゲストーゲンが最もよく使用されます:17-OPC、デポプロベラ、プロベラ、ファルルガル、デポスタット、メガスなどがタモキシフェンと併用または併用されません。
転移がある場合、プロゲスチン療法が無効の場合は、ゾラデックを処方することをお勧めします。
臓器温存治療は、治療前および治療中の詳細な診断が可能な専門施設でのみ実施可能です。診断機器だけでなく、形態学者を含む高度な資格を持つ人員も必要です。これはすべて、治療の非効率性を適時に検出し、その後の手術を行うために不可欠です。さらに、継続的な動的モニタリングも不可欠です。若年女性の微小子宮内膜がんに対する臓器温存ホルモン療法の可能性:プロゲストーゲン:17-OPKまたはデポプロベラとタモキシフェンの併用。中等度の分化度では、ホルモン療法と化学療法(シクロホスファミド、アドリアマイシン、フルオロウラシル、またはシクロホスファミド、メトトレキサート、フルオロウラシル)の併用が用いられます。
腫瘍の分化度が高度または中等度の患者には、ホルモン療法の処方が推奨されます。腫瘍の分化度が高い場合、子宮筋層への表層浸潤がある場合、腫瘍が子宮底部または子宮の上部2/3に局在している場合などです。50歳未満で転移のない患者には、ホルモン療法を2~3ヶ月間実施します。効果がない場合は、化学療法に切り替える必要があります。
治療の詳細


