疫学
治療の成功は、さまざまな臓器や肝臓でタンパク質と多糖類の複合体(アミロイド)の形成を引き起こす病気のタイムリーな診断に直接依存します。実際にわかるように、アミロイドーシスを特定したり確認したりすることは可能ですが、アミロイドーシスを仮定したり疑ったりすることは困難です。実際のところ、認識されていない症例の 80% 以上では、この病気は臨床的には肝臓の病理によって隠蔽されています。最も効果的な診断方法は生検です。
肝アミロイドーシスは、腎アミロイドーシスと比較すると、よりまれな問題です。同時に、肝臓病変のすべての症例は他の臓器の病変を伴います。ほとんどの場合、病理は主に肝三徴の構造部分に影響を及ぼし、これが症状の最小性と非特異性を決定します。肝細胞欠損および門脈圧亢進症の臨床的および形態学的像は、びまん性および小葉内タイプの病状に現れます。
以前の肝症状がなく、肝腫大が存在し、ネフローゼ症候群がない場合、肝生検が正当化されます。
びまん性肝障害は症例の約 25% で見られ、患者の 75% では門脈路のみが影響を受けます。
原発性アミロイドーシスは症例の 90% で肝臓に影響を及ぼしますが、二次性アミロイドーシスが肝臓に影響を与えるのは症例の 47% のみです。
単独の肝臓病変は非常にまれです。通常、腎臓(症例の約93%)、脾臓(72%)、心臓(57%)、膵臓(36%)、副腎(29%)、腸および肺(それぞれ21%)が同時に影響を受けます。
女性は男性のほぼ2倍の割合でこの病気にかかります。アミロイドーシス患者の平均余命は52~64歳です。
原因 肝アミロイドーシス
アミロイドーシスは、肝臓組織における複雑な多糖類-タンパク質複合体(アミロイド)の形成と蓄積を伴います。現在まで、一次病変の発生の問題は十分に研究されていません。二次病理に関しては、その出現は通常、次のような疾患に関連しています:
- 慢性感染プロセス(結核、梅毒、放線菌症);
- 化膿性炎症プロセス(微生物性心内膜炎、骨髄炎、気管支拡張症など);
- 悪性疾患(白血病、内臓癌、リンパ肉芽腫症)。
反応性アミロイドーシスは、同時性動脈硬化症、リウマチ性疾患(ベーチェレウ病、関節リウマチ)、乾癬、慢性炎症および多臓器プロセス(サルコイドーシスを含む)の患者に見られます。主なリスク要因:遺伝的素因、細胞性免疫障害、高グロブリン血症。
病因
肝アミロイドーシスの起源については多くの仮説があります。ほとんどの専門家は、異常タンパク症のバージョン、この病気の免疫学的性質および突然変異の性質、さらには局所的な細胞の発生に固執しています。細胞発生のバージョンには、細胞レベルで働く反応の変化(マクロファージの複合体によるアミロイドの線維前駆体の形成)が含まれますが、アミロイドは細胞構造の外側で形成および蓄積します。
異常タンパク質症のバージョンは、アミロイドが不適切なタンパク質代謝の産物であるという事実に基づいています。この問題の基本的な病因関係は、血漿中に粗く分散したタンパク質およびパラタンパク質画分の蓄積を引き起こす異常タンパク質血症と高フィブリノゲン血症にあります。
免疫学的バージョンによると、アミロイド形成は抗原抗体反応によって引き起こされ、組織崩壊産物または外来タンパク質が抗原として作用します。アミロイドの蓄積は、主に抗体形成と抗原の過剰存在の領域で見られます。
科学者らは、タンパク質合成の異常を引き起こす可能性のあるさまざまな突然変異誘発因子を考慮した突然変異理論を検討する最も妥当なバージョンを検討しています。
アミロイドは、多糖類と結合した球状および線維状タンパク質からなる複雑な低タンパク質です。アミロイドの蓄積は、血管網の内膜および外膜、実質臓器の間質、腺の構造などに影響を与えます。アミロイドの蓄積は機能的損傷を引き起こしません。小さな蓄積は機能障害を引き起こしませんが、アミロイドが大量に存在すると、肝臓の体積が増加し、臓器の外観が変化し、機能の欠如が発生します。
肝アミロイドーシスは、ディッセ腔へのアミロイド線維の沈着を特徴とし、通常は門脈周囲領域から始まりますが、小葉中心性である場合もあり、肝血管系にも沈着する場合があります。 [4]、 [5]重症の場合、アミロイドの沈着により肝細胞の圧萎縮が起こり、胆汁の通過が妨げられて胆汁うっ滞が生じたり、類洞が閉塞して門脈圧亢進症が生じたりすることがあります。 [6]、 [7]、 [8]
症状 肝アミロイドーシス
肝アミロイドーシスの臨床像は多様であり、アミロイド蓄積の強度、その生化学的特徴、病理学的過程の期間、臓器損傷の程度、およびその機能状態の違反によって異なります。
アミロイドーシスの潜伏期では、肝臓内のアミロイド蓄積が顕微鏡検査によってのみ検出できる場合、病気の最初の兆候は存在しません。臓器のさらなる発達と機能不全の増加に伴い、症状は進行します。
肝臓は徐々に厚くなり、大きくなります。触診の方法は変更されますが、臓器の境界は滑らかで痛みがありません。まれに、右側の肋骨下領域の痛み、消化不良、脾臓の肥大、皮膚、粘膜および強膜の黄色化、出血症候群を伴う病理があります。
肝アミロイドーシスの最も特徴的な症状は次のとおりです。 [9]、 [10]
- 肝臓におけるアミロイドの蓄積は、患者の 33 ~ 92% で肝腫大を引き起こします。
- 軽度の黄疸
- 門脈圧亢進症;
- 中等度から重度の胆汁うっ滞。
アミロイドーシスが 1 つの臓器だけに影響を与えることは非常にまれであるため、通常は追加の症状が存在します。
- 腎臓の損傷によりネフローゼ症候群や動脈性高血圧が進行し、さらに腎不全、浮腫、場合によっては腎静脈血栓症、白血球尿症、血尿、低タンパク血症、高窒素血症などを引き起こす場合。
- 心臓が冒されると、拘束型心筋症に似た状態が発症します(リズム障害、心肥大、心臓欠損の増加、衰弱と呼吸困難、浮腫、頻度は低いですが、腹腔および胸腔内の体液の蓄積、心膜炎)。
- 消化管が影響を受けると、巨舌症、脱力感、食道の蠕動運動、吐き気や胸やけ、便秘や下痢などが起こることがあります。
- 膵臓が冒されると、慢性膵炎の症状が現れます。
- 筋骨格系のメカニズムが関与している場合は、対称性多発性関節炎、手根管症候群、ミオパチーが発症し、神経系が影響を受けている場合は、多発性神経障害、麻痺、起立性低血圧、発汗量の増加、認知症が見られます。
病理学的反応が皮膚に広がると、顔、首、皮膚のひだに多数のワックス状のプラークが現れます。神経皮膚炎、紅斑熱、強皮症の症状が考えられます。
複数のアミロイド病変とさまざまな症状の組み合わせにより、肝アミロイドーシスの同定はさらに困難になり、包括的かつ完全な診断が必要となります。
フォーム
WHO の分類によれば、アミロイドーシスは 5 つのタイプに分類されます。
- AL (プライマリ);
- AA (二次);
- ATTR (遺伝性および老人性全身性);
- Aβ2M (血液透析患者の場合);
- AIAPP (インスリン非依存性糖尿病患者);
- AB (アルツハイマー病);
- AANF(老人性心房アミロイドーシス)。
肝臓の局所的なアミロイドーシスがありますが、より多くの場合、それは全身性病変であり、病理学的過程には腎臓、心臓、脾臓、神経系、および他の臓器や組織も関与します。
合併症とその結果
全身性アミロイドーシスは徐々に急性の病理学的過程を発症させ、最終的に死に至る可能性があります。最も一般的で生命を脅かす合併症は次のとおりです。
- 肺炎、腎盂腎炎、糸球体腎炎などの頻繁な感染症(細菌性、ウイルス性)病状。
- 慢性肝不全および腎不全。
- 慢性心不全(心筋梗塞に先行する可能性がある)。
- 出血性脳卒中。
静脈血栓症は、静脈壁へのタンパク質の蓄積および沈着の結果として発生します。影響を受けた血管の内腔は狭くなり、臓器不全が発症します。長期にわたる高タンパク血症を背景に、時間の経過とともに血管が完全に閉鎖することがあります。いずれの合併症も、死亡という好ましくない結果を招く可能性があります。
診断 肝アミロイドーシス
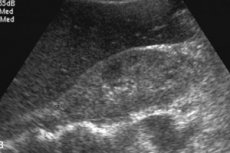
超音波検査で肝臓のアミロイドーシスを判断することは困難です。臓器の拡大が確認され、最も特異的な肝腫大は 15 cm を超えます。超音波の制御下で生検が実行され、これが診断の決定的な指標となります。特殊な針を使用して少量の肝臓組織を採取し、特殊な色素で染色して顕微鏡で検査すると、アミロイドの沈着を直接見ることができます。
最終的な診断は、肝臓や他の臓器の組織でアミロイド線維が検出された後にのみ行われます。遺伝的に決定されるアミロイドーシスのタイプは、家系図の注意深く遺伝医学的な検査によって決定されます。
差動診断
腎タンパク尿、拘束型心筋症、自律神経障害または末梢神経障害、および肝脊髄炎を組み合わせたすべての患者は、モノクローナルパラプロテインが存在しない場合でも、アミロイドーシスを疑う必要があります。病因が異なれば病変の治療法も大きく異なるため、アミロイドーシスの種類を確認することは非常に重要です。
組織学的診断には、コンゴレッドによる染色とその後の偏光による顕微鏡検査が含まれます。一度に複数の組織サンプルを生検することをお勧めします。染色結果が陽性となった場合は、前駆体タンパク質に対するモノクローナル抗体を用いた免疫組織化学的解析を行い、アミロイドの種類を同定します。
DNA 分析は、原発性アミロイドーシスと遺伝的に決定されたアミロイドーシスのさまざまなバリエーションを区別するために実行されます。アミロイド原線維は生検標本から単離され、個々のアミノ酸に隔離されます。
形質細胞の異常を判断するための追加の研究:
- 血液および尿の血清タンパク質の電気泳動。
- 遊離軽鎖のイムノアッセイ。
- 血清タンパク質の免疫固定(イムノブロッティング)。
- 骨髄穿刺とトレパノバイオプシー。
肝アミロイドーシスの診断は時間と労力を要するプロセスであり、専門医のさらなる注意力と診療所や検査室の高品質な設備が必要です。
連絡先
処理 肝アミロイドーシス
治療措置は、血中の既存のアミロイドタンパク質の濃度を低下させ(アミロイドーシスの原因を除去し)、適切な肝機能をサポートすることを目的としています。
続発性アミロイドーシスでは、炎症過程を遮断する必要があります(慢性感染症および自己免疫病態)。自己免疫疾患では、細胞増殖抑制剤の使用が推奨されます。慢性的な感染過程を排除するために、炎症の領域が外科的に除去されることがよくあります。多くの場合、このアプローチによりアミロイドーシスのさらなる進行を阻止し、肝機能を改善できます。
原発性アミロイドーシスでは、化学予防薬の使用と、場合によっては骨髄移植が必要です。
現在のガイドラインでは、新たにALと診断された患者の第一選択療法として、シクロホスファミド、ボルテゾミブ、デキサメタゾン(CyBorD)、ダラツムマブの併用が推奨されている。
ボルテゾミブはプロテアソーム阻害剤です。プロテアソームは、タンパク質毒性の軽減と、細胞の進行とアポトーシスを制御するタンパク質の制御に関与しています。アミロイドを生成する形質細胞は、軽鎖の毒性効果を軽減し、アポトーシスを防ぐためにプロテアソームに依存しているため、プロテアソーム阻害に特に敏感です。
ダラツムムマブは、形質細胞の表面に発現する膜貫通型糖タンパク質である CD38 に結合し、アポトーシスを誘導するモノクローナル抗体 (mAb) です。これは、CyBorD と併用した場合に AL アミロイドーシスの治療に特に承認されている唯一の薬剤です。 CyBorD-ダラツムムマブの有効性は非常に高く、患者の 78% が有意な血液学的応答 (完全応答または非常に良好な部分応答として定義) を達成しています。 CyBorDを受けた患者の小グループ(n = 15)の生存期間中央値は655日であったのに対し、他のメルファランデキサメタゾンベースの治療を受けた患者(n = 10)では178日でした。 4
しかし、これらの治療法には心毒性を含む多くの副作用があり、用量の減量または治療の中止、および効果は低いがより忍容性の高い他の治療戦略の使用が必要になります。
ダラツムマブと同様のCD38に対するモノクローナル抗体であるイサツキシマブは、ALの根底にある形質細胞異常の治療のために研究されています。
3 つのモノクローナル抗体ビルタミマブ、CAEL-101、AT-03 は現在、罹患臓器からのアミロイド原線維の除去について研究されています。これらの研究の結果は、臓器から軽鎖沈着原線維を除去することによって臓器機能が改善されるという仮説に対する直接的な証拠を提供することができるだろう。 [20]
肝機能をサポートするために、ウルソデオキシコール酸をベースにした薬が処方されています(例 - ウルソサン)。ウルソ-デオキシコール酸は、細胞膜の安定化を助け、アミロイド沈着によって引き起こされる胆汁うっ滞における有毒脂肪酸の悪影響を軽減し、正常な胆汁流出を回復するのに役立ちます。
さらに、対症療法や、神経系、心臓、腎臓などの他の重要な構造の機能のサポートも行われます。肝アミロイドーシス患者の支持療法には、心不全、不整脈、伝導障害、血栓塞栓症の治療など、さまざまな臨床的側面が含まれます。そして大動脈弁狭窄症の併発。
他の治療法は、アミロイドーシスの種類と体のどの部分が影響を受けるかによって異なります。治療には次のようなものがあります。 [21]
- 痛み止め、吐き気止め、腫れを抑える薬(利尿薬)など、症状を和らげる薬。
- アミロイドを減らすための薬。
- 腎臓透析。
- 肝臓移植。
肝臓は、血清中で測定されるTTR(トランスサイレチン、チロキシン(T4)輸送およびレチノール結合タンパク質に関与するタンパク質。トランスサイレチンは主に肝臓で合成され、不溶性アミロイド線維に凝集する傾向があるベータ鎖を豊富に含む)の95%を生成します。 。したがって、肝移植は歴史的に(1990年以来)、家族性型(ATTRv)の患者におけるアミロイド生成性TTRの主な原因を除去するための第一選択療法として提案されてきたが、ATTR-wt型では適応とされていない。病気の初期段階で若い患者に肝移植を行うと、20年生存率が高くなります。肝移植は、一部の変異では効果が高いようですが、V122I(心筋症に関連)などの他の変異では効果が低いようです。若年心筋症のATTRv患者では、肝臓と心臓の併用移植も可能であり、少数の患者グループに関する文献データは、この併用が心臓移植単独よりも予後が良いことを示唆している。
肝アミロイドーシスの患者は、アミロイドに蓄積する可能性がある強心配糖体やジルチアゼムやベラパミルなどのカルシウム拮抗薬の摂取は禁忌です。 ACE阻害剤とβアドレナリン遮断薬は注意して使用してください。
起立性低血圧では、心不全の代償不全を引き起こす可能性があることを考慮して、鉱質コルチコイドまたは糖質コルチコステロイドが処方されます。 α-アドレナリン作動薬ミドドリン(Gutron)も注意して使用されます。
神経障害には抗けいれん薬と抗うつ薬が適切です。
肝アミロイドーシスの場合には、医師は臓器の移植を考慮しなければなりません。
防止
肝アミロイドーシスの病因に関する情報が不足しているため、専門家はこの病気の特定の予防法を開発できません。したがって、主な取り組みは、疾患の発症を引き起こす可能性のある慢性病状のタイムリーな検出と治療に限定されます。家族内に局在性のアミロイドーシスの患者がいる場合は、計画的に医師の診察を受けて調剤検査を受けることをお勧めします。
一般に、予防策は、感染症、特に慢性化する傾向のある感染症をタイムリーに排除することに帰着します。結核や肺感染症などの発症を予防することが重要です。慢性型の自己免疫炎症過程の原因となり得る連鎖球菌感染症をタイムリーに検出し、適切な治療を行うことが重要です。猩紅熱、連鎖球菌性扁桃炎などについてお話します。
患者がすでに自己免疫疾患を患っている場合は、体系的に医師に相談し、病状の活動を観察し、医師の処方に従って必要な薬を適用し、適応症に従って用量を調整する必要があります。
予測
肝アミロイドーシス患者の予後は好ましくありません。この病気はゆっくりとしかし継続的に増加し、最終的には影響を受けた臓器の機能不全を引き起こし、特に臓器不全により致死的な結果を引き起こします。
全身性病変を有する患者は主に慢性腎不全の発症により死亡しますが、場合によっては血液透析または継続的な外来腹膜透析によりそのような患者の予後が改善される場合もあります。血液透析を受けている患者の生存率は、その種類に関係なく、他の全身性病状や糖尿病を患っている人々の生存率と比較できます。
血液透析中の主な死亡原因は、心血管系による合併症の発症です。
肝移植は長い間、この病気の主要な治療法の1つと考えられており、最も楽観的な生存率は年齢が50歳を超えない患者で観察されます(ただし、病理学的プロセスが短命であり、BMIが良好であるという条件で)普通)。末梢神経障害を伴う肝アミロイドーシス患者の予後はやや不良です。


