疫学
先進国では、産科医療のレベルが高いため、シーハン症候群はまれであり、その頻度は 50 年間で 10 万人の女性あたり 10 ~ 20 件から女性の下垂体機能低下症全体の 0.5% にまで減少しました。
欧州内分泌学会によると、出産時に多量の出血を経験した女性の4%に、下垂体前葉の軽度の損傷の症状が見られます。中等度のシーハン症候群の兆候は8%に診断され、循環血液量減少性ショック後の女性の50%に重度の産後下垂体機能低下症が認められます。
2012 年の国際薬物疫学レジストリ KIMS (ファイザー国際代謝データベース) には、成長ホルモン欠乏症 (GH) の患者が 1,034 人記載されており、女性患者の 3.1% の症例ではこの病状の原因がシーハン症候群でした。
産後下垂体機能低下症は、発展途上国および発展途上国の女性にとって深刻な脅威となります。例えばインドでは、20歳以上の出産経験のある女性におけるシーハン症候群の有病率は2.7~3.9%と推定されています。
原因 シーハン症候群
シーハン症候群のすべての原因は、出産時の出血による循環血液量の急激な減少と血圧の低下によって発症する血液量減少性ショックの結果です。
大量出血(800ml以上)により、臓器への血液供給と酸素供給が阻害されます。そして、まず第一に脳への影響が懸念されます。シーハン症候群は、脳内で最も重要なホルモンの合成を担う下垂体の損傷によって発症します。
最も大きな影響を受けるのは、前葉である下垂体のホルモン産生細胞です。妊娠中は胎盤ホルモンの影響を受けて、この腺の大きさは推定値によると120~136%増加します。特に、乳腺の発達と乳汁産生の準備に必要なプロラクチンを合成する細胞であるラクトトロポサイトの肥大と過形成が見られます。
危険因子
産婦人科医は、シーハン症候群の発症の危険因子として以下を挙げています。
- 妊婦の血液凝固障害(特に血小板減少症)
- 末梢組織の浮腫(視床下部ホルモンのバソプレシンが活性化され、血管緊張と血圧が上昇する)
- 妊娠性高血圧(高血圧)
- 妊娠高血圧症候群(高血圧およびタンパク尿)
- 溶血(赤血球の破壊、最もよく見られるのは腎不全に伴う)の増加。
前置胎盤(胎盤が早期に剥離する)の場合、また多胎妊娠(双子または三つ子)や急速な(激しい)陣痛の場合、出産中に出血したり、シーハン症候群を発症したりするリスクが高まります。急速な(激しい)陣痛の場合は、羊水による肺血管の塞栓症が起こる可能性があります。
病因
シーハン症候群の病因は、下垂体組織の低酸素症と壊死に関連しています。下垂体前葉の脆弱性を高める主な要因は、門脈系と門脈の毛細血管吻合網を介した血液供給の特殊性です。重度の出血と血圧低下により、肥大した下垂体前葉の局所的な血流が阻害されます。ショック状態に伴う下垂体栄養血管の痙攣は、酸素欠乏と虚血性壊死を引き起こします。
その結果、下垂体は以下の栄養ホルモンを十分な量生成できなくなります。
- 細胞タンパク質合成を活性化するソマトトロピン(STH)は、炭水化物代謝と脂質加水分解を調節します。
- プロラクチン(黄体刺激ホルモン)は乳腺と黄体の発達と機能を刺激します。
- 卵胞刺激ホルモン(FSH)。卵胞の成長と子宮組織の増殖プロセスを促進します。
- 排卵を司る黄体形成ホルモン(LH)
- 副腎皮質刺激ホルモン(ACTH)は副腎皮質によるコルチコステロイドの産生を活性化します。
- 甲状腺の分泌機能を調節する甲状腺刺激ホルモン(TSH)。
症状 シーハン症候群
シーハン症候群では、下垂体で産生されるホルモンの不均衡により、特定の下垂体ホルモンの分泌欠乏の程度に応じてさまざまな症状が引き起こされます。
損傷した下垂体細胞の量によって、急性型と慢性型に分類されます。急性型は下垂体前葉に重大な損傷が生じており、出生後すぐに症状が現れます。慢性型では、検出される損傷は小さく、症状は出生後数ヶ月から数年経ってから現れることもあります。
シーハン症候群の最も一般的な初期症状は、無乳症、つまり乳汁分泌の減少です。エストロゲンの長期的欠乏により、出産後も月経周期が適切な時期に再開せず、乳腺が縮小し、膣粘膜が薄くなります。また、ゴナドトロピン欠乏は、無月経、稀発月経、性欲減退として現れます。一部の女性では月経が再開し、再妊娠の可能性が高まります。
シーハン症候群における甲状腺刺激ホルモン欠乏症の特徴的な症状には、疲労感、体温調節障害(寒さへの耐性低下)、皮膚の乾燥、脱毛、爪の脆弱化、便秘、体重増加などがあります。これらの症状は通常、徐々に進行します。
ソマトトロピン欠乏症の影響は、筋力の低下、体脂肪の増加、インスリン感受性の亢進に限られます。急性型と慢性型のいずれにおいても、尿崩症の兆候、すなわち激しい喉の渇きと利尿作用(尿量の増加)が現れる場合があります。
シーハン症候群の症状には、二次性副腎機能不全、すなわちACTH欠乏症の徴候も含まれます。これには、全身の緊張低下と体重減少、低血糖(血糖値の低下)、貧血、低ナトリウム血症(ナトリウム濃度の低下)が含まれます。このホルモンの欠乏は、失神や起立性低血圧を伴う慢性的な低血圧、そしてストレスへの反応不能を引き起こします。また、色素沈着の低下や皮膚のしわ(生後数週間から数ヶ月)も観察されます。
重度の感染症や外科的介入により、緊急の医療を必要とする副腎機能不全の悪化が発生します。
診断 シーハン症候群
シーハン症候群の診断は通常、臨床的特徴と患者の病歴、特に分娩中の出血の有無や分娩に伴うその他の合併症の有無に基づいて行われます。授乳の問題や出産後の無月経に関する情報は、この症候群の重要な兆候です。
下垂体ホルモン(TSH、ACTH、FSH、LH、T4)、コルチゾール、エストラジオールのレベルを確認するには血液検査が必要です。
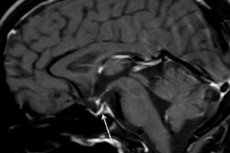
機器診断(脳のコンピュータ断層撮影(CT)または磁気共鳴画像(MRI)を用いた検査)により、下垂体の大きさと構造を調べることができます。初期段階では下垂体は腫大し、時間の経過とともに萎縮し、「空洞トルコ鞍」などの病理学的診断徴候が現れます。これは、脳底部の下垂体窩における下垂体の消失を示すもので、スキャンによって明らかになります。
処理 シーハン症候群
シーハン症候群の治療は、卵巣、甲状腺、副腎皮質の刺激ホルモンの合成類似体を使用した生涯にわたるホルモン補充療法です。
したがって、ACTHとコルチゾールの欠乏は、グルココルチコイド(ヒドロコルチゾンまたはプレドニゾロン)の服用によって補われます。チロキシン製剤(レボチロキシン、テトラヨードチロニンなど)は甲状腺ホルモンを補充し、血清中の遊離チロキシン濃度の血液検査データは、投与量の調整に役立ちます。
エストロゲン欠乏症は通常は経口避妊薬の使用によって治りますが、シーハン症候群の女性は閉経までこれらのホルモンを服用しなければなりません。
内分泌専門医は、血中ホルモン濃度が適切にコントロールされていれば、通常は副作用はないと指摘しています。ホルモン剤の投与量が多すぎたり少なすぎたりすると、副作用が生じる可能性があります。そのため、この症候群の患者は経過観察を受け、定期的な検査とホルモンの血液検査を受ける必要があります。



 [
[