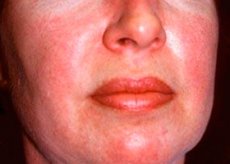
多発性筋炎と皮膚筋炎は、筋肉(多発性筋炎)または筋肉と皮膚(皮膚筋炎)の炎症性および変性性変化を特徴とする、まれな全身性リウマチ性疾患です。最も特異的な皮膚症状はヘリオトロープ疹です。
筋障害は対称性で、近位骨盤帯筋群の筋力低下、軽度の圧痛、そしてそれに続く萎縮がみられます。合併症としては、内臓障害や悪性腫瘍が考えられます。診断は、臨床所見と、酵素値の測定、MRI、筋電図検査、筋生検による筋機能障害の評価に基づきます。治療にはグルココルチコイドが用いられ、免疫抑制剤や静脈内免疫グロブリンとの併用が行われる場合もあります。
女性は男性の2倍の頻度で発症します。この病気はどの年齢でも発症する可能性がありますが、最も多く発見されるのは40歳から60歳、小児では5歳から15歳です。
皮膚筋炎と多発性筋炎の原因は何ですか?
この疾患の原因は、遺伝的に素因のある人における筋組織に対する自己免疫反応であると考えられています。この疾患は、家族歴が重篤な場合や特定のHLA抗原(DR3、DR52、DR56)を保有している場合に多く見られます。誘因として考えられるのは、ウイルス性筋炎と悪性腫瘍です。筋細胞からピコルナウイルスに類似した構造が検出されるという報告があり、さらに、ウイルスは動物において同様の疾患を引き起こす可能性があります。悪性腫瘍と皮膚筋炎の関連(多発性筋炎よりもはるかに低い頻度)は、腫瘍の増殖が、腫瘍と筋組織の共通抗原に対する自己免疫反応の誘発によって、この疾患の発症の誘因となる可能性を示唆しています。
骨格筋の血管壁には、IgM、IgG、そして補体第3成分の沈着が見られます。これは特に小児の皮膚筋炎に特徴的な所見です。多発性筋炎の患者は、他の自己免疫疾患を発症することもあります。
皮膚筋炎および多発性筋炎の病態生理学
病理学的変化には、様々な重度の炎症を背景とした細胞の損傷と萎縮が含まれます。上肢、下肢、および顔面の筋肉は、他の骨格筋に比べて損傷の程度が軽度です。咽頭および上部食道の内臓筋、そして頻度は低いものの心臓、胃、腸の損傷は、上記の臓器の機能不全につながる可能性があります。横紋筋融解症によるミオグロビン濃度の上昇は、腎障害を引き起こす可能性があります。特に抗合成酵素抗体を持つ患者では、関節や肺の炎症性変化も発生する可能性があります。
皮膚筋炎および多発性筋炎の症状
多発性筋炎の発症は急性(特に小児)または亜急性(成人に多い)の場合があります。急性ウイルス感染は、時に発症に先行したり、発症の誘因となることもあり、最も一般的な症状は近位筋の筋力低下または皮膚発疹です。疼痛は筋力低下よりも軽度に現れます。多発性関節痛、レイノー現象、嚥下障害、肺疾患、全身症状(体温上昇、体重減少、筋力低下)が現れる場合があります。レイノー現象は、結合組織疾患を併発している患者によく見られます。
筋力低下は数週間から数ヶ月かけて進行することがあります。しかし、臨床的に筋力低下が現れるには、少なくとも筋線維の 50% が影響を受けている必要があります (したがって、筋力低下の存在は筋炎の進行を示しています)。患者は、腕を肩より上に上げること、階段を上ること、または座った姿勢から立ち上がることが困難になることがあります。骨盤筋と肩甲帯の筋の重度の筋力低下により、患者は車椅子または寝たきりになる場合があります。首の屈筋が影響を受けると、枕から頭を上げることができなくなります。咽頭と上部食道の筋肉が影響を受けると、嚥下障害や逆流が生じます。下肢、上肢、顔面の筋肉は通常影響を受けません。しかし、四肢の拘縮が生じることがあります。
皮膚筋炎でみられる皮膚発疹は、通常、色が濃く、紅斑性です。眼窩周囲の紫色の浮腫(ヘリオトロープ発疹)も特徴的です。皮膚発疹は皮膚よりわずかに盛り上がり、滑らかまたは鱗状になることがあります。発疹の部位は、額、首、肩、胸、背中、前腕、すねの下部、眉毛、膝周辺、内果、指節間関節および中手指節関節の背側、外側(ゴットロン症状)です。爪の付け根または爪周囲の充血がみられることもあります。指の外側の皮膚に、ひび割れを伴う剥離性皮膚炎が発生することがあります。一次性の皮膚病変は後遺症なく治まることが多いですが、色素沈着、萎縮、瘢痕、白斑などの二次的な変化を引き起こすことがあります。特に小児では皮下石灰化が生じることがあります。
患者の約30%に多発性関節痛または多発性関節炎が発現し、しばしば浮腫や関節液貯留を伴います。しかし、関節症状の重症度は軽度です。Jo-1やその他の合成酵素に対する抗体が検出された場合、これらの症状はより多く発生します。
多発性筋炎では、他のリウマチ性疾患(特にSLEおよび全身性強皮症)と比較して、内臓(咽頭および上部食道を除く)の病変は比較的まれです。まれに、特に抗合成酵素症候群においては、間質性肺炎(呼吸困難および咳嗽)として発症することがあります。不整脈や伝導障害が生じることもありますが、通常は無症状です。血管炎を併発している小児では、消化器症状がより多く見られ、吐血、下血、腸穿孔などがみられることがあります。
どこが痛みますか?
多発性筋炎の分類
多発性筋炎には5つのタイプがあります。
- 原発性特発性多発性筋炎は、あらゆる年齢で発症する可能性があり、皮膚には影響を及ぼしません。
- 原発性特発性皮膚筋炎は、原発性特発性多発性筋炎に似ていますが、皮膚が侵されます。
- 悪性腫瘍を伴う多発性筋炎および皮膚筋炎は、あらゆる年齢の患者に発生する可能性がありますが、その発症は高齢者や他の結合組織疾患の患者に最も多く見られます。悪性腫瘍の発症は、筋炎発症の2年前から2年後までの間に観察されることもあります。
- 小児多発性筋炎または皮膚筋炎は全身性血管炎を伴います。
- 多発性筋炎および皮膚筋炎は、他の結合組織疾患、最も一般的なのは進行性全身性硬化症、混合性結合組織疾患、および SLE の患者にも発生する可能性があります。
体幹筋炎を多発性筋炎のグループに含めることは誤りです。なぜなら、多発性筋炎は慢性特発性多発性筋炎と同様の臨床症状を特徴とする別の疾患だからです。しかし、体幹筋炎は高齢期に発症し、しばしば体の末端部(例えば、上肢と下肢)の筋肉を侵し、持続期間が長く、治療への反応が悪く、典型的な組織学的所見を呈します。
皮膚筋炎および多発性筋炎の診断
近位筋の筋力低下を訴える患者には、圧痛の有無にかかわらず、多発性筋炎が疑われます。ヘリオトロープまたはゴットロン徴候に類似した発疹を訴える患者、および多発性筋炎の症状と皮膚筋炎に一致する皮膚病変が併存する患者には、皮膚筋炎の評価が必要です。多発性筋炎および皮膚筋炎の臨床症状は、全身性強皮症、あるいはまれに全身性エリテマトーデス(SLE)や血管炎の症状に類似することがあります。以下の5つの基準を可能な限り多く満たすことで、診断の確実性は高まります。
- 近位筋の筋力低下;
- 特徴的な皮膚の発疹;
- 筋肉組織酵素(クレアチンキナーゼ、またはその活性の増加がない場合はアミノトランスフェラーゼまたはアルドラーゼ)の活性の増加。
- 筋電図またはMRIにおける特徴的な変化;
- 筋組織生検における特徴的な組織学的変化(絶対基準)。
筋生検により、体幹筋の筋炎やウイルス感染による横紋筋融解症など、臨床的に類似する病態を除外することができます。組織学的検査で明らかになる変化は様々ですが、慢性炎症、筋変性および再生の病巣が典型的に認められます。毒性のある治療を開始する前に、正確な診断(通常は組織学的検証による)が必要です。MRI検査により、筋肉内の浮腫および炎症の病巣を検出し、その部位を標的とした生検を行うことができます。
臨床検査は、疾患の存在を確定したり、逆に疑いを解消したりできるだけでなく、重症度、他の類似病態との併発の可能性、合併症の診断にも有用です。一部の患者で抗核抗体が検出されることもありますが、この現象は他の結合組織疾患によく見られます。患者の約60%は、核抗原(PM-1)または胸腺細胞全体とJo-1に対する抗体を保有しています。Jo-1に対する抗体は、線維化性肺胞炎、肺線維症、関節炎、レイノー現象などの抗合成酵素症候群の特異的マーカーであることが知られていますが、疾患の病因における自己抗体の役割は依然として不明です。
クレアチンキナーゼ活性の定期的な評価は、治療のモニタリングに有用です。しかし、重度の筋萎縮を伴う患者では、慢性活動性筋炎が存在するにもかかわらず、酵素活性が正常である場合があります。MRI、筋生検、またはクレアチンキナーゼ活性の上昇は、多発性筋炎の再発とグルココルチコイド誘発性ミオパチーの鑑別に役立つことがよくあります。
多くの患者が未診断の悪性腫瘍を抱えているため、一部の著者は、60歳以上の皮膚筋炎および多発性筋炎の成人患者全員に対し、以下のスケジュールでスクリーニングを行うことを推奨しています。乳房、骨盤、直腸の検査(便潜血検査を含む)を含む身体検査、血球計算、血液生化学検査、マンモグラフィー、癌胎児性抗原検査、尿検査、胸部X線検査。臨床的に悪性腫瘍の証拠がない若年患者におけるこのようなスクリーニングの必要性に疑問を呈する著者もいます。
何を調べる必要がありますか?
どのように調べる?
皮膚筋炎および多発性筋炎の治療
炎症が治まるまで、身体活動を制限する必要があります。グルココルチコイドが第一選択薬です。病気の急性期には、成人患者にはプレドニゾロン(経口)を1日40~60 mgの用量で処方する必要があります。クレアチンキナーゼ活性の定期的な測定は、有効性の早期指標です。ほとんどの患者では、筋力の増加に続いて6~12週間以内に低下または正常化が認められます。酵素活性が正常化した後、プレドニゾロンの用量を減らします。最初は1週間かけて1日あたり約2.5 mgずつ減らし、その後はより急速に減らします。筋酵素活性の増加が再発した場合は、ホルモンの用量を再び増やします。回復した患者はグルココルチコイドなしでもかまいませんが、成人患者ではほとんどの場合、長期のグルココルチコイド療法(1日あたりプレドニゾロン10~15 mg)が必要です。小児に対するプレドニゾロンの初期用量は、1日1回30~60 mg/m 2です。小児では寛解が 1 年を超えて続く場合、グルココルチコイド療法を中止することができます。
場合によっては、高用量のグルココルチコイドを投与された患者は突然の筋力低下を経験しますが、これはグルココルチコイドミオパチーの発症に関連している可能性があります。
グルココルチコイド治療への反応が不十分な場合、グルココルチコイド性ミオパチー、あるいはプレドニゾロンの減量または中止を必要とするその他の合併症を発症した場合は、免疫抑制剤(メトトレキサート、シクロホスファミド、アザチオプリン、シクロスポリン)を使用する必要があります。患者によっては、メトトレキサートのみ(通常はRA治療で使用される用量を超える用量)を5年以上投与されることもあります。薬物療法に抵抗性のある患者には、静脈内免疫グロブリンが有効な場合がありますが、その使用は治療費の増加につながります。
原発性腫瘍および転移性腫瘍に伴う筋炎、ならびに体幹筋の筋炎は、通常、グルココルチコイド療法に対してより抵抗性を示します。悪性腫瘍に伴う筋炎は、腫瘍切除後に寛解する可能性があります。
皮膚筋炎および多発性筋炎の予後はどのようなものですか?
治療を受けた患者の半数以上で、5年以上にわたる長期寛解(さらには臨床的回復)が認められます。小児では、この数値はさらに高くなります。しかし、再発はいつでも起こり得ます。全体的な5年生存率は75%で、小児ではさらに高くなります。成人の死因は、重度かつ進行性の筋力低下、嚥下障害、栄養低下、誤嚥性肺炎、または肺感染症による呼吸不全です。多発性筋炎は、心臓や肺に損傷がある場合、より重篤で治療が困難になります。小児では、腸の血管炎が原因で死亡することがあります。この疾患の一般的な予後は、悪性腫瘍の存在によっても左右されます。



 [
[