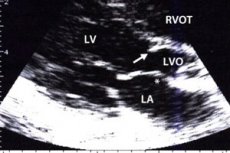
肥大症および脳室中隔の領域におけるその他の心筋障害では、大動脈への血液輸送が損なわれています。この領域は大動脈弁の領域に先行するため、この狭窄は大動脈流出路狭窄症として特徴付けられます。左心室の収縮の瞬間の患者では、めまい、意識の障害、呼吸によって明らかにされる血流を防ぐ閉塞があります。治療は、疾患の形と臨床像に応じて、保守的または外科的である可能性があります。
特発性肥大症性大動脈狭窄症
大動脈下狭窄の原因を特定できず、病理の発達と損傷と遺伝性の要因との関係を見つけることも不可能である場合、そのような疾患は特発性と呼ばれます。
この用語は、不特定の原因または自発的狭窄によって引き起こされる狭窄に適用されます。
肥大症性骨骨狭窄症といえば、それらは筋原線維の異常な過成長を意味します。
- 環状肥大性狭窄(運河を覆う襟の外観があります);
- 半陰症(隔壁または僧帽弁リーフレットに尾根の形状があります);
- トンネル狭窄(左心室流出路全体が影響を受けます)。
解剖学的バリアント
分離または他のものと組み合わせて発生する多型大動脈狭窄症のバリアントのスペクトルがあります。彼らは次のとおりです:
ほとんどの患者では、閉塞は、介入中隔に付着した膜または左心室流出路を包囲することによって引き起こされます。 [3]、 [4]、 [5]その位置は、大動脈弁の直下から左心室まであらゆるものにすることができます。大動脈弁フラップの基部は、移動度を制限し、左室流出管を拡張するこの大動脈組織に関与していることに注意してください。
疫学
亜多重型大動脈狭窄症は、乳児や新生児に見られるまれな状態ですが、大動脈狭窄の2番目に一般的なタイプです。すべての先天性心臓欠陥の約1%(10,000人の新生児に8人)と、左心室流出路のすべての固定閉塞性病変の15%から20%の原因です。
先天性大動脈狭窄症の小児は、亜多重型の大動脈狭窄症の症例の10〜14%を持っています。男性ではより一般的であり、症例の65%から75%の範囲です。 [6]、 [7]男性と女性の比率が2:1。亜多重型の大動脈狭窄の有病率は、成人のすべての先天性心疾患の6.5%です。 [8]
1バルブ大動脈狭窄は、症例の50〜65%で他の心臓奇形と関連しています。 [9] 35人の患者の報告で、付随する病変が発見されました。
- 心室中隔欠損(VSD)(20%)
- 開いている動脈管(34%)
- 肺狭窄(9%)
- 大動脈の縮前(23%)
- 他のさまざまな病変(14%)
すべての左心室流出路閉塞の中で、症例の約10〜30%で大動脈下狭窄が発生します。
問題は男性でより頻繁に発生することに注意してください(女性よりも1.5倍から2倍頻繁に)。
ほとんどの場合、関連する病理は次のとおりです。
- 二極大動脈弁;
- 大動脈弁狭窄;
- 大動脈の縮小;
- 動脈管を開いています。
- 局所中隔欠損;
- ファロットのテトラッド。
- 完全な房室通信。
先天性大動脈骨狭窄症の患者の約20〜80%は、同時性心臓病を患っており、50%は大動脈弁不全の増加と診断され、これは血行動態異常に関連しています。さらに、大動脈下狭窄は、シェンの複合体の症状の1つである可能性があります。
先天性隔離狭窄症は、生涯の初年度に生まれたばかりの乳児と子供の間でまれな診断です。古い年齢では、病理学は長年にわたって潜在的に存在する可能性があります。しかし、30歳以降、先天性骨骨狭窄症は事実上まれです。 [10]
原因 大動脈下狭窄症
多くのメカニズムは、遺伝的因子、他の心臓病変で見られる血行動態異常、または流出路の乱流を増加させる左室流出路の形態など、固定亜価値大動脈狭窄の発生に寄与します。 [11]さまざまな欠陥(主に先天性)は、大動脈下狭窄の発症を引き起こす可能性があります。特に、そのような欠陥には以下が含まれます。
- 前区画バルブリーフレットの介入膜、僧帽弁、または脈絡膜の異常への不適切な付着。
- 機械的閉塞の形成による僧帽弁の肥厚、肥厚;
- 軟骨との前僧帽弁葉の孤立した発散。
- パラシュート型の僧帽弁の曲率。
- 左心室流出路筋肉の肥大。
- 左心室流出路などを循環させる大動脈弁の下の線維性肥厚など。
病理学的変化は、大動脈弁と近くの解剖学的元素(例えば、僧帽弁)の両方に影響する可能性があります。 [12]
危険因子
大動脈下狭窄の発症における主な要因は、遺伝的障害です。疾患の遺伝性形態には、心筋収縮タンパク質の形成の欠陥が伴います。特発性自発性骨骨狭窄症は珍しいことではありません。
ほとんどの場合、専門家は次の誘発要因に言及しています。
- 局所中隔肥大;
- 糖尿病、甲状腺中毒、肥満、アミロイドーシスを含む代謝障害。
- 化学療法治療;
- アナボリック、麻薬の使用;
- 結合組織疾患;
- 細菌およびウイルスの感染性病理;
- 慢性アルコール依存;
- 放射線治療を含む放射線被曝;
- スポーツハート症候群。
脳室中隔の肥大による大動脈狭窄症は、持続的な循環不全につながります。収縮活動の瞬間、バルブリーフレットと中隔の間に血液が輸送されます。圧力が不十分なため、左心室流出管の僧帽弁の重複が大きくなります。その結果、大動脈への十分な血流がなく、肺流出が妨げられ、心臓と脳の不足が発生し、不整脈が発生します。
病因
先天性骨骨狭窄症は、大動脈弁の亜型空間の構造変化、または僧帽弁などの近くの構造の発達欠陥を伴います。
膜性横隔膜狭窄症は、左心室流出管に穴を開けるか、左心室流出路の半分以上を減少させる線維性溝の折り畳みを伴う円形線維の存在によるものである可能性があります。膜のオリフィスは5〜15 mmという大きさです。ほとんどの場合、膜は大動脈弁の繊維環のすぐ下、またはわずかに下に局在しており、右冠状動脈または非環状リーフレットの下の脳室中隔の前部僧帽弁葉の底に沿って付着しています。
弁骨骨狭窄症は、大動脈弁の5〜20 mmの局在化を伴う弁型の線維性肥厚によって現れます。
線維筋下狭窄症は、大動脈弁の10〜30 mmの「襟」と同様の特異な肥厚であり、前部僧帽弁リーフレットと接触して、左心室の流出路を「左室の流出路」のように「抱きしめます」。狭窄は、最大20〜30 mmの非常に長くなる場合があります。病理学は、しばしば、バルブ繊維環の形成不全とバルブフラップの側面の変化の背景に対して検出されます。
トンネル型の大動脈下狭窄は、この病理の最も顕著なタイプであり、左心室流出管の筋肉組織における激しい肥大変化を特徴としています。その結果、長さ10〜30 mmの繊維性筋肉のトンネルが形成されます。その内腔は狭くなり、これは密な繊維層に関連しています。左心室の筋肉組織は、肥大した、内膜虚血、線維症、時には脳室中隔の重度の肥大(後部左心室壁と比較して)、および組織学的に混乱した筋肉繊維が認められています。 [13]
症状 大動脈下狭窄症
臨床像の重症度と強度は、消化管の狭窄の程度に依存します。次の最初の兆候が最も頻繁に記録されます。
- ぼやけた意識、半壊れ、失神の定期的なエピソード。
- 息切れ;
- 胸痛(エピソードまたは一定);
- 心臓のリズム乱れ;
- 頻脈、動pit;
- めまい。
症状は、身体的運動、過食、アルコール消費、興奮、恐怖、身体の位置の突然の変化の背景に対して増加します。心臓の痛みは狭心症に似ていますが、大動脈下狭窄では、硝酸塩(ニトログリセリン)を服用することは緩和されませんが、痛みを増加させます。
時間が経つにつれて、病理は悪化します。健康診断の過程で、頂端振戦の左側の変位では、その分岐または増幅が検出されます。頸動脈の領域では、脈拍は2波(二波)であり、急速に増加しやすいです。静脈圧が増加するため、頸部血管は拡張され、下肢が膨張し、腹腔(腹水)および胸膜(水吸引術)に液体が蓄積します。
心雑音は、頂点を越えて収縮期の瞬間に耳を傾け、その音は直立位置、吸入時、呼吸中に増加します。 [14]
合併症とその結果
専門家は、大動脈下狭窄の過程のいくつかの特徴的なバリエーションについて話します:
- 良性のコースでは、患者は満足のいくものであると感じており、診断測定は明らかな血行動態障害を明らかにしません。
- 複雑な進歩的なコースでは、患者は衰弱の増加、心臓の痛みの増加、休息時の呼吸困難の出現、定期的な失神の増加に注意してください。
- ターミナルステージには、重度の循環不全の発生が伴います。
最も一般的な合併症は次のとおりです。
- 心臓の動pitの試合(頻脈);
- エクストラシーストール;
- 心房細動と脅迫的脳塞栓症;
- 突然の心停止。
診断 大動脈下狭窄症
最初の診断段階では、症候学が評価され、心臓ゾーンと首の血管の触診とパーカッションが行われます。大動脈骨狭窄症では、左心室肥大と触診 - 尖端の揺れのぼやけにより、心臓境界のパーカッシブな拡大を左に検出することが可能です。触診は、頸動脈に沿って継続して、心塩基で収縮期の振戦を明らかにする可能性があります。
聴診は明らかにします:
- 右側の2番目のcost間空間を支配する粗い収縮期雑音は、頸動脈に放射されます。
- 大動脈弁での拡張期の逆流のつぶやき。
以下のテストをお勧めします。協力的な出血のリスクと失血量のリスクを予測するための凝固造影、血小板数。さらに、貧血を検出するために血液学的研究が行われます。 [15]
機器の診断には、そのような技術の使用が含まれます。
- 胸部X線は、心臓のサイズを測定します(大動脈骨狭窄症では、心臓が拡大し、球状の構成を獲得します)。
- 心電図(大動脈骨狭窄症には、左心室筋肥大の兆候、深部Q歯の出現、ST減少、第1標準鉛、v5、v6;拡大した左トリウムの結果として2番目と3番目の鉛の拡張Pが検出されます);
- ホルター心電図(頻脈攻撃、心房細動、外筋腫を検出するため);
- 超音波(大動脈下狭窄症では、中隔は左心室壁よりも1.25倍厚くなっています。左心室容量が不十分であり、大動脈弁を通る血流が低下し、収縮期の中央の後者の閉鎖、左心房拡張);
- 心臓プロービング(吸気呼吸の圧力の変化、最終的な拡張期圧の増加);
- 心室造影、血管造影(左心室収縮時に大動脈に逃げる血液の問題が明らかになります)。
差動診断
場合によっては鑑別診断は、左心室からの流出障害を伴う先天性骨下狭窄症と肥大性心筋症の間で行われます。得られた診断結果は、その後の治療的戦術の選択において重要な役割を果たします。
連絡先
処理 大動脈下狭窄症
困難は、大動脈下狭窄症の外科的介入は常に非常に外傷性であり、寿命リスクの増加と関連しているという事実にあり、保存療法は常に望ましい効果につながるとは限りません。
心臓の負荷を減らし、左心室機能を改善するために、そのような薬物を処方することが可能です。
- β遮断薬(アナプリン、40から160 mgに毎日の投与量が徐々に増加する);
- カルシウムチャネル阻害剤(イソプチン);
- 抗不整脈薬(Cordarone)。
炎症性合併症(心内膜炎など)の脅威がある場合、セファロスポリン抗生物質(セファゾリン)またはアミノグリコシド(アミカシン)による抗生物質療法が処方される場合があります。 [16]
これらの一般的な薬物は、大動脈骨狭窄症には推奨されません:
- 利尿薬;
- ニトログリセリン;
- 心糖質体;
- ドーパミン、アドレナリン;
- 血管拡張薬。
深刻な進行中の病理学と保存療法による効果の欠如により、心室と大動脈に50 mm Hgを超える圧力の違いがあるため、医師は特に外科的介入の問題を提起することができます。
- 心室性能を最適化するための僧帽弁補綴物。
- 筋切除 - 中隔機能を改善するための心筋の切除。
代替方法の中で、ペースメーカーまたは除配給器の配置がリードしています。
治療は、患者の食事の変化によって必然的に補完されます。推奨:
- しばしば食べ過ぎずに小さな食事を食べる。
- 塩、動物脂肪、スパイシーなスパイス、調味料を除外します(血管系を改善するため)。
- 液体摂取量を1日あたり800〜1000 mlに制限します。
- アルコール飲料、ソーダ、コーヒー、強いお茶を排除します。
- 食事では、ベジタリアンスープ、おridge、煮込み野菜、沸騰した海魚、乳製品、果物、ナッツ、ハーブ、ベリーを好みます。
亜多重型の大動脈狭窄における外科的介入の基準とタイミングは議論の余地があります。これらの患者への早期介入は、術後の再発の高い発生率、後期再手術、および閉塞緩和後の大動脈逆流の発症によって相殺されます。 [17]、 [18]
- 平均ドップラー勾配が30 mm Hg未満で、左心室肥大がない小児および青年では、亜価値の大動脈狭窄の治療は、非介在性と医療モニタリングで構成されています。
- 50 mmHg以上のドッププレロメトリック平均勾配を持つ小児および青年には、外科的治療が必要です。
- 30〜50 mm Hgの平均ドップラー勾配の小児および青年は、症候性狭心症、失神、または運動時に呼吸困難があるが、無症候性であるが、安静時または運動ECG、または古い年齢で変化を発症する場合、外科的介入を検討することができます。診断時。 [19]
- 大動脈逆流の予防だけでは、通常、外科的介入の基準ではありません。ただし、逆流の進行と悪化は、外科的介入の兆候です。
防止
大動脈下狭窄の遺伝性形態は予防することはできませんが、疾患の合併症の発症を防ぐために予防策が必要です。まず、身体活動を監視し、過負荷を避け、筋力トレーニングや心筋の肥大変化のリスクを高める他のエクササイズを避ける必要があります。
次の変更が検出された場合、運動はキャンセルされます。
- 左心臓の明確な圧力の不一致。
- 顕著な心筋肥大。
- 心室または室内症の不整脈;
- 直接的な親relativeの突然の死の症例(死因は未定である可能性があります、または肥大した心筋症の結果)。
体系的な衰弱、めまい、身体的運動の痛み、息切れの場合、医師に相談する必要があります。遺伝的素因の場合、超音波、心電図、心室造影などの年間予防診断を受けることをお勧めします。生涯を通じて、塩と動物の脂肪の制限、および分数の食事で食事を追うことが望ましいです。身体活動を絶えず監視し、筋力トレーニングで体を過負荷にしないでください。医師とトレーナーの監督の下でのみ運動します。
大動脈下狭窄の発症を防ぐための予防的測定は、心臓のアテローム性動脈硬化、リウマチ、および感染性炎症性病変の予防と密接に関連しています。心血管疾患の患者は、心臓専門医とリウマチ専門医による定期的な監視が必要なため、健康診断の対象となります。
予測
大動脈骨狭窄症は、長年にわたって顕著な症状がなく、時には潜在的です。明らかな臨床症状が現れると、致死結果を含む合併症の可能性が大幅に増加します。主な不利な兆候の中で:
- 狭心症;
- シンコープ前、失神;
- 左心室障害(通常、このような状況では、5年生存率は2〜5年です)。
乳児と小児は頻繁に監視され(4〜6か月ごとに)進行速度を理解するために進行率を理解する必要があります。これは進行性疾患であるためです。
大動脈下膜切除手術を受けた患者の生存は優れていますが、左心室流出路勾配が時間とともにゆっくりと増加するため、これらの患者は監視する必要があります。術後患者の長期フォローアップが重要です。ほとんどの患者は、再発のために人生のある時点で再手術を必要とします。 [20]
再手術率の増加の独立した予測因子は次のとおりです。
- 女性の性別
- 時間の経過に伴う瞬間的なLVOT勾配進行のピーク
- 術前と術後のピーク瞬時のLVEF勾配の違い
- 術前のピーク瞬間LV勾配80 mm Hg以上。
- 診断時に30歳以上
左心室機能不全の発症とタイムリーな外科的介入により、5年生存が症例の80%以上で報告され、症例の70%で10年生存が報告されています。複雑な骨骨狭窄症には不利な予後があります。


