骨芽細胞腫は、良性または悪性のいずれかであり、異なる骨格骨を損傷する可能性のある腫瘍プロセスです。最初は、病理はギガントセルラー腫瘍と呼ばれていました(1912年以降)、10年後、スチュワート博士は骨炎腫という名前を提案しました。そして、1924年にのみ、ルサコフ教授は、新生物の細胞組成にもっと完全に対応する洗練された用語「骨芽細胞腫」を導入しました。
今日、骨芽細胞腫は、広範な血管ネットワークを備えた軟部組織腫瘍である真の新生物と見なされています。唯一の正しい治療オプションは、健康な組織内の腫瘍の除去であり、時には骨移植と同時に同時にです。 [1]
疫学
世界中の骨腫瘍の発生率は0.5〜2%の範囲です。米国統計によると、骨肉腫(症例の約34%)、軟骨肉腫(27%)、およびユーイングの腫瘍(18〜19%)が最も一般的です。脊柱腫、線維肉腫、線維腫、組織球腫、巨大細胞腫瘍、および血管肉腫はあまり一般的ではありません。
発生率は年齢と高度に相関しています。したがって、腫瘍の成長の最初の急増は、思春期(約16歳)で検出され、中年で2回目の急増が検出されます。
骨芽細胞腫は比較的一般的な腫瘍です。それはすべての骨新生物の約2〜30%で発生します。女性はより多くの場合影響を受けますが、主に18歳から40歳までの男性も影響を受ける可能性があります。12歳未満の子供はめったに影響を受けませんが、この年齢期間でさえ、発生率は除外されません。骨芽細胞腫の家族的および遺伝的症例の説明があります。
ほとんどの場合(約75%)腫瘍は長い管状の骨に見られますが、平らで小さな骨がはるかに少なくなります。
長い管状の骨では、エピメタフィシスは主に影響を受け、小児期にはメタシシスが影響を受けます。新生物は、骨端と関節軟骨の領域に芽生えません。非常にまれに問題が発言に見られることはほとんどありません(症例の0.5%未満)。
医学の発生により、骨芽球腫瘍の発生率は安定したままですが、死亡率は大幅に低下していることに注意してください。病理学の主な原因と最も可能性の高い原因は、電離放射線の影響であると考えられています。したがって、高用量の放射線療法を受けた人と、放射性同位体を注射された患者(診断または治療目的)でリスクが増加します。他の一般的な病因要因には、不利な生態学と遺伝が含まれます。 [2]
原因 骨芽細胞腫
骨芽細胞腫は、骨格のほぼすべての部分に現れることができる病理学的に変化した細胞の焦点です。構造の異常にもかかわらず、健康な組織のように、病理細胞は分裂し続けます。それらの構造は、直接影響を受ける骨の特性とその典型的な機能の置換を伴う規範とは大きく異なります。病理学的に変化した悪性細胞は、腫瘍の体積が増加する結果として、制御されていない、しばしば急速な増殖の傾向を獲得します。以前は正常な骨組織は、新生物の構造によって変位することができ、個々の病理細胞を分離し、血液またはリンパで他の遠い解剖学的ゾーンに輸送できます。このようにして、転移が形成されます。
悪性骨芽細胞腫の供給源は、体のあらゆる部分(内臓の腫瘍を含む)にあるあらゆる悪性新生物であることが知られています。プロセスの拡散方法は転移です。しかし、ほとんどの骨芽細胞腫(良性と悪性の両方)は、最初に同じ場所に現れて発達する主要な新生物です。
一般に、骨芽細胞腫は、現時点では正確な原因が確立されていない多因子腫瘍です。新生物の発生の条件には、次のようなものが含まれます。
- 免疫不全状態;
- 先天性組織の変化;
- 変異原性環境の影響;
- ホルモンの変化;
- 付随する病理と怪我(外傷はしばしば前manesisに存在します)。
危険因子
骨芽細胞腫の形成の原因に関する正確なデータが不足しています。しかし、専門家は、骨腫瘍病理学のリスクの増加に関連する多くの要因の関与を示唆しています。
- 遺伝。多くの場合、腫瘍プロセスの傾向は遺伝的に決定されます。特に、これはLeigh Fraumeni症候群の場合である可能性があります。これは、癌性腫瘍や肉腫を含むさまざまな新生物の発生を素因としています。
- パジェット病。この病気は1つ以上の骨に影響を与え、腫瘍前の病理に属します。この障害のある患者では、骨が濃くなり、同時に脆くなり、頻繁な病理学的骨折が生じます。骨肉腫は、重度のパジェット病の症例の約8%で発生します。
- 複数の骨の過成長、エキソストーズ。
- 複数の骨軟骨腫(遺伝性を含む)。
- 複数のエンコンドロマ(リスクは小さいが、まだ存在している)。
- 放射線被曝(他の腫瘍プロセスの治療に使用される強い放射線と放射性ラジウムとストロンチウムの影響を含む)。
リスクの特別なカテゴリーには、小児期および若年年齢の放射線治療が含まれ、60灰色を超える用量があります。
専門家は、非イオン化光線、特に、電力線、携帯電話、家庭用家電から形成されるマイクロ波と電磁放射が、骨芽細胞腫のリスクを伴わないという事実に注意を向けています。
病因
骨芽細胞腫の外観と発達の病原性の特徴は完全には理解されていません。これは、病理学の複雑さによるものです。腫瘍形成の基本的な原因は、免疫系の不適切な機能による細胞分化の失敗です。これにより、新生物の特性を決定し、構造的に未熟な細胞に似ている「間違った」、未分化細胞からなる腫瘍の成長が生じます。細胞構造が正常に近いがそうでない場合、それは良性骨芽球腫腫であると言われています。細胞の構造の顕著な変化により、腫瘍は悪性プロセスに起因します。このような新生物の場合、抗原細胞の折り畳み、制御されていない成長、細胞分裂の変化が典型的です。細胞構造の特異性の喪失とともに、機能も苦しみます。とりわけ、悪性骨芽細胞腫は、近くの健康な組織への浸潤のプロセスによって、良性骨芽細胞腫とは異なります。良性の骨新生物では、健康な構造に芽を出すことはなく、急速な成長や体全体に広がる傾向はなく、腫瘍分解の産物による任意の自己破壊と中毒の傾向はありません。
病理の良性に関係なく、すべての場合に骨構造が破壊されます。その結果、罹患した骨セグメントは脆弱で脆くなります。多くの場合、医師に目を向ける理由は、最小限の負荷でも発生する病理学的骨折です。
注意することが重要です:プロセスの良性は常に条件付き状態です。なぜなら、悪性化のリスクがあり、良性の焦点が変換されるため、悪性骨芽細胞腫が発生するからです。
症状 骨芽細胞腫
骨芽細胞腫の臨床像は、主に病理学的プロセスの局在と段階に依存しています。原則として、腫瘍は次の特徴によって特徴付けられます。
- 新生物は孤独です。
- 主に下肢または上肢の管状骨に影響します。
- 平らな骨ではあまり見られません。
- 影響を受けるセグメントにはしつこい痛みがあります。
- 病理学的焦点に対する皮膚と血管パターンが増加します。
- 病気の肢が変形されます(局所的な体積の増加)。
- 骨芽細胞腫に最も近い関節または手足全体の仕事は妨げられています。
- 特徴的な「羊皮紙のクランチ」で、パルパトリーで圧縮された焦点を決定しました。
一般に、症状は局所的および一般的な症状に分けることができます。局所的な症状は視覚的に検出されます - 特に、骨の断片の曲率または膨らみの存在を見ることができます。病理学的焦点に対する皮膚の変化にも注意が払われます。血管パターンが明らかに現れ、組織は腫れたり平らになったりします。腫瘍は触診することができます - 多くの場合、それは痛みがありませんが、特徴的な構造を持っています。悪性腫瘍は通常、塊状で構成が不規則です。
隣接するジョイントは動きが制限されている可能性があり、持続的に痛みを伴います。血管と神経幹の圧縮により、感度はしばしば損なわれ、持続的な腫れが現れます。リンパ系も反応します。近くのリンパ節が拡大します。
一般的な症状は、悪性骨芽細胞腫腫の方が典型的であり、体の中毒のプロセスによるものです。患者は持っているかもしれません:
- 発熱、熱性条件。
- ガントネス;
- 一定の弱さ;
- 眠気または不眠症、食欲障害;
- 夜間の過度の発汗;
- 崩壊。
また、骨芽球腫瘍のごく一部がありますが、これは通常小さく、臨床的には明らかではありません。それらは、他の理由で放射線またはイメージング研究中に偶発的な発見になります。
骨芽細胞腫の骨化の最初の兆候
- 新生物の成長を加速します。
- 疼痛症候群の増加。
- 直径への破壊的な焦点の拡大、または細胞間隔形態の溶解型への変換。
- 比較的長い領域にわたる皮質層の崩壊。
- 破壊的な焦点の構成の明確さの喪失。
- 髄質をブロックするために使用される閉鎖プレートの崩壊。
- 骨膜反応。
骨芽細胞腫の悪性腫瘍は、臨床的および放射線学的指標に基づいており、腫瘍組織の形態学的診断によって必然的に確認されています。
最初は良性の新生物の脱骨崩壊化に加えて、主要な悪性骨芽細胞腫もあります。実際、そのような腫瘍は骨形成病因の肉腫の一種です。
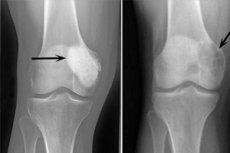
悪性骨芽細胞腫の位置は、良性プロセスと同じです。 X線撮影は、透明な輪郭のない骨組織の破壊的な焦点を明らかにしています。皮質層の破壊が拡張され、しばしば軟部組織構造に芽が出ることが観察されます。
悪性骨芽細胞腫と骨形成型の骨砕屑性肉腫を区別する兆候:
- 患者の主に高齢の年齢。
- 鮮やかな症状の少ない;
- より有利な長期予後。
小児の骨芽細胞腫腫
小児期の骨芽細胞腫はまれです。100万人の子供につき1症例または3症例しかありません。すべての小児患者の中で、10〜15歳以上の患者が支配的であることに注意する必要があります。
科学者は、小児の骨芽細胞腫の正確な原因に名前を付けることはできません。おそらく、病理は、遺伝的因子と同様に、子供の体の集中的な成長に関連しています。
また、放射性曝露(特に放射線療法)、化学療法(細胞症の服用)などの考えられる原因の兆候もあります。多くの化学療法薬は、骨細胞の遺伝物質を破壊し、腫瘍形成の発生につながる可能性があります。
さらに、骨芽細胞腫のリスクは、両側網膜芽細胞腫やLi-フラウメニ症候群などの特定の先天性症状の小児で高くなっています。因果関係は、パジェット病にも存在します。
また、大多数の子供(約90%)では、医師が上記の危険因子を検出できないことも知られています。
特定の腫瘍の特徴、その局在化、診断時の拡散の程度、治療の適時性、および新生物の除去の完全性に依存するため、小児期の骨芽球閉鎖の経過を予測することは困難です。
骨芽細胞腫の治療の質は、過去2〜30年で大きな進歩を遂げました。治療プロトコルが組み合わされ、治療率は70〜80%以上増加しました。腫瘍プロセスが根本的に外科的に除去され、効果が十分な化学療法で統合された場合、好ましい結果が言えます。良性骨芽球腫腫の子供は、回復の可能性が最も高いです。
治癒した患者の特定の数値が発表されると、一般的な数字のみが表示されます。特定の子供の可能性を正確に予測して決定する統計はありません。 「回復」という用語は、現代の治療アプローチが再発の長期的な欠如を確実にすることができるため、主に「体内の腫瘍プロセスの欠如」として理解されています。ただし、望ましくない副作用と後期合併症の可能性を忘れてはなりません。したがって、その複雑さに関係なく、どの治療も高品質のリハビリテーション対策に流れ込むはずです。さらに、子どもたちは依然として長い間整形外科ケアを必要としています。
フォーム
骨組織新生物の分類は非常に広いです。主に、細胞構造、腫瘍プロセスの形態学的特性の変動に注意が払われます。したがって、腫瘍は2つのカテゴリに分けられます。
- 骨形成(骨細胞に基づいて形成);
- 新生遺伝子(他の細胞タイプの影響下で骨で形成されます - たとえば、血管または結合組織構造など)。
骨の骨芽細胞腫は主に良性新生物です。しかし、それにもかかわらず、それはしばしば攻撃的な成長を抱えており、骨組織の破壊と薄化に寄与し、外科的介入を義務付けています。同時に、巨大細胞骨芽球腫も悪性です。
臨床的および放射線学的パラメーターと形態学的絵に応じて、骨芽細胞腫の3つの基本的な形態が際立っています。
- 細胞形態は主に高齢者に見られ、発達が遅いことを特徴としています。診断は、健康な骨ゾーンからの腫瘍の焦点を臨床的に描写する可能性がなく、濃厚でゴツゴツした腫れを明らかにしています。
- まず第一に、嚢胞性の形態は痛みで現れます。パルパトリーでは、「羊皮紙のクランチ」の症状が決定されます。視覚的には、滑らかに凸状のドーム型の構成の骨腫瘍が認められています。
- 溶解型は、病理学のまれなバリアントと見なされ、主に思春期に検出されます。腫瘍のプロセスは十分に迅速に発達し、患者は触診を含む痛みに悩まされ始めます。
手足、rib骨、脊椎の管状の骨はやや頻繁に影響を受けますが、巨大な細胞腫瘍は骨格のほぼすべての骨に形成されます。下顎の骨芽細胞腫腫は、上顎の2倍の頻度で発生します。触知的に、柔らかいゾーンを伴う密な新生物が認められています。患者の最も一般的な苦情:食べ物を噛むときに出血して不快感を生み出す膨らみの存在。問題が進むにつれて、顎関節の機能障害によって補完されます。管状の骨の中で、腫瘍は大腿骨と脛骨によく影響します。大腿骨の骨芽細胞腫は主に中年の人々に見られます。この病気には、対応する関節の機能障害が伴い、la行が発生し、新生物上の皮膚は顕著な血管パターンで覆われています。
上記の分類に加えて、病理学の中心的および周辺形態がありますが、それらの間に形態学的な違いはありません。末梢骨芽球腫腫は歯肉局所化を持ち、中心形態は骨に発生し、その中に複数の出血が存在することによって区別されます(したがって、中心骨芽細胞腫の2番目の名前は茶色の腫瘍です)。茶色の外観は、ヘモシデリンの形成と崩壊する赤血球の沈着によるものです。
悪性骨新生物は、開発の次の段階を経ています。
- 3〜5 cmのT1病巣は、骨と1つの筋根性セグメント内にあります。
- T2焦点は、骨のコースに沿って10 cm以下に伸びていますが、1つの筋膜のケースを超えて延びていません。
- T3病巣は、1つの筋根性症例の範囲を残し、近くの症例に芽を出します。
- 皮膚または神経血管幹からのT4病巣の芽。
同様に、リンパ節の関与の程度と転移の拡散が分類されます。
合併症とその結果
骨芽細胞腫の合併症の中には、新生物の活性の増加があります。これは、特に長い静かな時代の背景に対してしばしば発生します。そのような場合、腫瘍プロセスの悪性変性、または近くの敏感な解剖学的構造への発芽について話している:
- 神経幹への広がりは、大口径神経への影響により、神経障害性疼痛症候群の発生を引き起こします。このような痛みは、従来の鎮痛薬を服用した後に実際に排除されていないため、文字通り患者を使い果たします。
- 血管への広がりは、突然の大量の出血と血腫の形成によって複雑になる可能性があります。
合併症は除外されていません。これには、近くの関節の機能の違反が伴います。このような状況における骨芽細胞腫の成長は、筋骨格メカニズムの適切な機能をブロックします。
骨芽細胞腫の最も一般的な合併症は、患部の病理学的骨折と考えられています。骨組織が非常に壊れやすく不安定になるため、問題はわずかな外傷性の影響でさえも発生します。
さらに、専門家は、悪性骨芽球腫の特徴的な特定の一般的および局所的副作用についても話します。
- 遠くおよび近くの転移の形成。
- 腐敗生成物による身体の中毒。
最初の診断測定後しばらくの間転移が検出された場合、それは進行中の治療と新生物の進行の非効率性を示します。
別の合併症は、化学療法または骨芽細胞腫骨の焦点の照射による新しい腫瘍または一般的な病理の出現です。
診断 骨芽細胞腫
骨芽細胞腫を検出するために使用される診断方法は次のとおりです。
- 病理学的に変化した領域の外部検査と触診を含む臨床。
- X線(示されている場合は、標的および斜めのX線撮影);
- 断層撮影(コンピューター化または磁気共鳴画像法を使用);
- 放射性同位体;
- 形態学的、穿刺または骨道生物中に得られた生体材料の組織学的、組織化学的、細胞学的分析を含む。
- 研究室。
医師は、病気の歴史を慎重に研究し、最初の兆候を決定し、痛み症候群の場所と種類、その特徴を指定し、以前の検査と治療手順の結果を考慮し、患者の一般的な状態のダイナミクスを評価します。長い管状の骨の病理が疑われる場合、専門家は、腫れの存在、より近い明瞭度の運動制限、および神経症状、筋肉の脱力、低栄養の存在に注意を払っています。内臓を慎重に調べて、転移が拡散する可能性があることが重要です。
すべての患者は、タンパク質およびタンパク質画分、リンとカルシウム、シアル酸を測定して、一般的な血液および尿検査を服用します。また、ホスファターゼの酵素活性を決定し、定義テストを実施し、C反応性タンパク質の指標を研究する必要があります。骨芽細胞腫をミルマと区別する必要がある場合、患者は病理学的ベンス・ジョーンズタンパク質の存在のために尿検査に合格します。
放射線診断は、骨芽細胞腫の診断の基本です。義務的な任命されたレビューと標的X線、高品質の断層撮影、場所、病理学的焦点の種類、他の組織や臓器への広がりを明確にすることができます。 CTのおかげで、軟部組織の状態と必要な面で最も薄い骨構造を明確にし、病理学的破壊の深い焦点を特定して、骨の制限内のそれらのパラメーターを記述し、周囲の組織への損傷の程度を決定することができます。
同時に、MRIは最も有益な診断手順と見なされます。これは、放射線撮影とCTの両方よりも多くの利点があります。この方法では、最も薄い組織層を調べて、空間的な3次元画像を使用して病理学的なチャグの写真を形成することができます。
必須の機器診断は、形態学的研究で表されます。生体材料が評価され、吸引および骨道生物症の間、または骨セグメントと新生物の切除中に得られます。穿刺生検は、特別な針と放射線コントロールを使用して行われます。
次のX線徴候は、骨芽細胞腫の典型的なものと見なされます。
- 多孔性制限;
- 薄い骨分類のタイプにおける骨溶解の均一性。
- 独特の「泡」の構造を持つ偽嚢胞性の存在。
この放射線学的絵には、一次または二次反応性の骨形成術がないことが伴います。皮質層の薄化と萎縮が検出されます。
集中的な血管発芽の結果としての悪性のタイプの骨芽細胞腫腫は、静脈停止の増加を伴います。血管の変化は、豊富な血管新生を伴う新生物の出現を持っています。
差動診断
骨芽細胞腫を特定することは非常に困難な場合があります。異なる年齢の患者の骨形成性肉腫と骨嚢胞との疾患の診断の鑑別診断中に問題が発生します。統計によると、症例の3%以上で、骨芽球菌は骨形成肉腫と間違え、症例のほぼ14%が骨嚢胞と間違えられていました。
表は、これらの病理の主な兆候を要約しています。
|
インジケーター |
骨芽細胞腫 |
骨形成骨形成肉腫 |
骨嚢胞 |
|
発生率の最も一般的な年齢 |
20〜30歳 |
20〜26歳 |
14歳未満の子供 |
|
位置 |
エピメタフィシール地域 |
エピメタフィシール地域 |
メタディアフェイシスエリア |
|
骨再構成 |
重度の非対称バルジ。 |
小さな横膨張 |
紡錘形の膨らみ。 |
|
破壊的な焦点の構成 |
輪郭は明確です |
輪郭はぼやけており、明確にはありません |
輪郭は明確です |
|
脊髄の状態 |
閉鎖プレートで覆われています |
新生物との境界線で開いています |
変更はありません。 |
|
皮質層の状態 |
薄く、繊維状、不連続。 |
薄め、台無しに |
薄く、平ら |
|
硬化現象 |
非定型 |
現在 |
非定型 |
|
骨膜反応 |
不在 |
「Periosteal Visor」タイプの方法に存在します |
不在 |
|
骨端の状態 |
層は薄く、波状です。 |
初期段階では、骨端の一部はそのままのままです |
変更はありません。 |
|
近くの骨セクション |
変更はありません。 |
骨粗鬆症の兆候 |
変更はありません。 |
義務的な注意には、患者の年齢、病理学の持続時間、影響を受ける焦点の位置、表に示されているその他のamniction情報などの指標が必要です。
骨芽細胞腫がそのような病理学的プロセスと混同される場合、次の診断エラーが最も一般的です。
- 動脈瘤嚢胞(長い管状の骨の甲状腺または薄膜に局在する);
- 単軸タイプの繊維状骨骨形成(主に小児期に現れ、骨球のない骨の湾曲を伴う);
- 副甲状腺症の骨過成(健康な骨領域からの焦点の明確な描写はなく、明確な骨の膨らみはありません);
- 孤立した癌骨転移(湾曲した「食べられた」輪郭を備えた破壊的な病巣によって特徴付けられます)。
良性の骨芽球腫腫は常に変化し、悪性になることができることに留意することが重要です。悪性腫瘍の原因はまだ正確に決定されていませんが、科学者は外傷とホルモンの変化(妊娠中など)がそれに寄与すると考えています。いくつかの観察によると、一連のリモート放射線処理が繰り返されると悪化も起こりました。
骨化の症状:
- 新生物は急速に成長し始めます。
- 痛みは悪化しています。
- 破壊的な焦点のサイズが増加し、細胞間知識相が溶解相に移行します。
- 皮質層が崩壊しています。
- 破壊的な焦点の輪郭は不明瞭になります。
- ロックプレートが崩壊しています。
- 骨膜の反応があります。
原発性悪性新生物(骨形成骨砕屑性肉腫)および悪性骨芽球腫瘍の分化の過程で、病理学の期間、ダイナミクスの放射線絵の評価に特に注意が払われます。主要な悪性新生物のX線画像では、骨芽細胞腫に典型的な骨突起はありません。骨橋はなく、不明瞭な輪郭を持つ硬化領域を検出できます。しかし、悪化しても、しばしば閉鎖プレートの小さな領域があり、これは健康な骨セグメントの障壁として機能していました。
連絡先
処理 骨芽細胞腫
骨芽細胞腫患者の唯一の正しい治療法は手術です。最も穏やかな介入は、腫瘍プロセスの発達の初期段階で行われ、罹患した組織の切除を表し、空洞が移植片をさらに充填することを表します。移植片は、患者の別の健康な骨から採取されます。このような介入は最も有利で、外傷性が低いですが、場合によっては根本的ではありません。罹患した骨断片と新生物の切除は、より信頼性の高い方法と見なされ、腫瘍の再成長の可能性を最小限に抑えます。
特に悪性化しやすい、または既に悪性、部分的または完全な切断が起こりやすい大きさの無視された骨芽細胞腫の場合、しばしば考慮されます。
一般に、骨芽細胞腫の外科的治療の戦術は、病理学的焦点の場所、拡散、攻撃性に応じて選択されます。
腫瘍が長い管状の骨に影響を与える場合、これらのタイプの外科的介入に注意を払うことをお勧めします。
- 良性、遅延プロセス、細胞構造を備えた病巣、およびエピメタフィスの周辺の焦点のためのアロ形成術または自己形成を伴うエッジ切除。金属ネジによる固定。
- 細胞骨芽細胞腫が骨直径の中央に広がると、顆の3分の2、部分的には甲状腺と関節表面が切除されます。欠陥は、関節軟骨同種移植で満たされています。ネクタイボルトとネジでしっかりと固定されています。
- 上尖の崩壊の場合、全長または病理学的骨折に沿った減衰があり、関節切除を伴う分節切除や異種移植片の欠陥を埋めるなどの戦術が使用されます。セメント付きロッドで固定されています。
- 近位大腿骨領域における病理学的骨折と骨芽細胞腫の悪性化の場合、全股関節形成術が行われます。
- 膝の関節ゾーンで端を切除した場合、固定を伴うallopolysubstance移植の技術が使用されます。拡張されたチタン茎を使用した総血管施設は、その後の放射線治療を確保するためにしばしば好まれます。
- 病理学的焦点が脛骨の遠位端に位置する場合、骨塑性足首関節を伴う切除が行われます。 Talus Boneが影響を受けた場合、伸長の関節固定で染色されます。
- 子宮頸部脊椎病変では、C1 およびC2 椎骨への前方アクセスが行われます。前外側アクセスが望ましい。 Th1-th2レベルで、3番目のcost間空間に斜めの胸骨切開術を伴う前方アクセスが使用されます(血管は慎重に下に移動します)。腫瘍が3-5胸部の体に影響を与える場合、3番目のrib骨の切除を伴う前外側のアクセスが行われます。肩甲骨は筋肉組織を遮断することなく後方に移動します。骨芽細胞腫がTh11And L2の間の胸腰部領域で見られる場合、選択の手術は右側胸部肺臓器切開術です。仙骨の上部3椎骨の前部へのアクセスはより困難です。血管幹と尿管の慎重な排水を伴う前外側後腹膜の右側にアクセスすることをお勧めします。
- 椎体がひどく破壊された場合、または病理が胸部および腰椎の脊椎のアーチ領域に広がっている場合、この場合、脊椎のトランスペディクラ - トランスラミナー固定が行われ、その後、破壊された椎骨がさらなる自己形成術で除去されます。
- 骨芽細胞腫腫の良性形態が眉と坐骨の骨で検出された場合、病理学的に変化したセグメントは、骨移植なしで健康な組織内で除去されます。寛骨臼の床と屋根が影響を受ける場合、切除はさらに骨移植で行われ、欠陥を交換し、胞子症の留め具で固定します。
- 腸骨、胸骨、または坐骨神経骨が影響を受けた場合、構造的同種移植片、移植骨合成、セメントベースのプラスチック挿入、および人工空洞への補綴ヘッドの再配置を伴うアロプラスト術を行います。
- 仙骨とl2 Are罹患した場合、病理学的に変化した下仙骨断片の後部アクセス切除(S2 )、interior side retroperitoneal方法からの腫瘍の除去の除去を含む2段階の介入が行われます。
特定の状況ごとに、医師は、治療結果を改善し、患者の通常の生活の質を確保するために最新の技術を適用する可能性を考慮するなど、外科的介入の最も適切な方法を決定します。
防止
骨芽細胞腫の特定の予防はありません。まず第一に、これはそのような腫瘍の発生の原因に関する研究が不十分なためです。多くの専門家は、主な予防ポイントの中で骨システムに対する外傷の予防を強調しています。しかし、骨新生物の形成に対する外傷の直接的な影響の証拠はなく、多くの場合、外傷は既存の腫瘍プロセスに注意を引くだけであり、病理学的焦点の起源に明らかな重要性はありませんが、同時にその成長に寄与する可能性があります。
骨芽細胞腫がしばしばイオン化放射線にさらされていた骨にしばしば形成されることを忘れてはなりません。たとえば、他の腫瘍プロセスの治療を目的として。放射性誘発性新生物は通常、放射線曝露から3年以内に発生します。
非固有の予防措置には次のものが含まれます。
- 悪い習慣の排除;
- 健康的なライフスタイルをリードする。
- 品質と持続可能な栄養;
- 中程度の通常の身体活動;
- 怪我の予防、体内の病理学的プロセスのタイムリーな治療、免疫の安定化。
予測
病理学的骨折は、しばしば骨組織の患部で発生します。この場合、根本的な治療方法が使用されることを条件に、良性新生物は、病理学的焦点の再発と悪性腫瘍の可能性は除外されていませんが、好ましい予後を持っています。焦点が積極的な成長と顕著な骨破壊によって特徴付けられる場合、良性骨芽細胞腫の不利な結果は除外されません。このような腫瘍は、病理学的骨折の発達と骨機能の重大な障害を伴う骨セグメント全体を迅速に破壊する可能性があります。そのような患者は、骨組織欠損の外科的置換に問題があり、骨折の非治癒に関連する合併症に問題があります。
子供と成人の両方における悪性骨芽細胞腫腫のすべてのバリアントの平均5年生存率は70%であり、これは非常に良いと見なすことができます。したがって、多くの場合、そのような新生物は非常にうまく癒されていると結論付けることができます。もちろん、腫瘍プロセスのタイプ、その段階、病変の程度、悪性腫瘍などのポイントも非常に重要です。
明らかに、最大の脅威をもたらすのは悪性骨芽細胞腫です。この状況では、早期発見、アクセス可能な外科的局在化、化学予防剤および放射線療法への焦点の感度の場合にのみ、好ましい予後について話すことができます。


