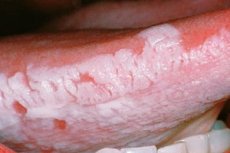
毛状白板症は、皮膚表面の毛髪の成長とは関連がなく、粘膜の疾患であり、病変部が糸状の白い絨毛で覆われ、組織学的検査でのみ観察されます。口腔毛状白板症は、1984年に初めて報告されたエプスタイン・バーウイルス感染症に関連する粘膜疾患で、免疫抑制状態の人にのみ発生します。視覚的には、左右対称に位置するプラークのように見えます。
疫学
この疾患は1984年にアメリカでエイズに感染した患者で初めて発見され、記述されました。科学者たちはこの2つの病態の関連性を解明してきました。毛状白板症の症例の4分の1から半数はHIV感染者に見られました。
2003年における一般人口における口腔白板症の全体的な有病率は1.7~2.7%の範囲であった[ 1 ] 。
毛状白板症は、HIV感染の同性愛男性(38%)の方が、HIV感染の異性愛男性(17%)よりも多く発症する。[ 2 ] ブラジルで実施された横断研究では、リオグランデ連邦大学病院のHIV/AIDSクリニックで治療を受けた成人患者の臨床検査、面接、医療記録から収集したデータが報告されている。300人が追跡調査された(2006年4月から2007年1月)。これらの患者のうち、51%が男性で、平均年齢は40歳だった。最も多かった病変はカンジダ症(59.1%)で、次いで毛状白板症(19.5%)であった。
危険因子
HIV感染、エイズ、その他の免疫不全の原因に加え、日常的な大量の喫煙や乱交的な同性愛関係も危険因子となります。患者の中には、潰瘍性大腸炎、その他の消化器疾患、そして口腔、性器、眼の粘膜に影響を及ぼすベーチェット症候群の患者も含まれていました。遺伝的素因も重要であり、糖尿病や口腔内の機械的損傷(義歯、詰め物など)も病態の一因となります。
病因
口腔毛状白板症の病因は複雑で、エプスタイン・バーウイルスの持続複製と毒性、全身性免疫抑制、そして局所宿主免疫の抑制が相互作用して生じます。[ 5 ] ウイルスはまず咽頭の基底上皮細胞に感染し、そこで複製期に入り、放出されて生涯にわたってヒトの唾液中に残存します。また、B細胞にも侵入し、増殖に好ましい状況(多くの場合、免疫機能不全)が生じるまで、無期限に潜伏状態を維持することができます。
症状 毛髪性白板症
毛状白板症は、長期間にわたり無症状のまま進行することがあります。最初の兆候は、舌の側面、舌の上部と下部、そしてまれに頬の内側、歯茎、軟口蓋に白い苔が現れることです。苔は主に左右対称で、一時的に消失しますが、その後再び出現することがあります。[ 6 ] 舌にひび割れが生じたり、軽度の疼痛、知覚異常、味覚の変化が生じることもあります。[ 7 ]
病変は徐々に白っぽい縞模様へと融合し、健康なピンク色の縞模様と交互に現れます。外観は洗濯板のように見えます。口腔および舌の毛状白板症はゆっくりと進行し、個々のひだは粘膜上に最大3mmの大きさのプラークを形成します。その境界は不明瞭で、擦過しても除去できません。
上記の局在に加えて、病理は、女性では外陰部、クリトリス、子宮頸部、男性では機械的および化学的要因によって促進される陰茎の頭に発生する頻度がはるかに低い(30歳以上の男性に発生)。
HIV による毛状白板症には、体重減少、夜間の過度の発汗、原因不明の下痢、発熱発作が伴います。
ステージ
毛状白板症は粘膜の長期にわたる慢性の栄養障害であり、いくつかの段階を経ます。
- 細胞の増殖、増殖;
- 扁平上皮の角質化;
- 細胞の硬化(病的な再生、結合組織による置換)。
フォーム
白板症にはいくつかの種類があります。
- 平ら - ヘラで取り除くことができない、ギザギザの輪郭を持つ、わずかに粗いフィルムのように見えます。
- いぼ状 - 直径2〜3 mmで白っぽい色の隆起した斑点によって表されます。
- びらん性 - 最初の 2 つの白板症の病巣にびらんの形で現れ、時にはひび割れとなる。
- 喫煙者白板症またはタッパイナー白板症は、硬口蓋と軟口蓋の領域に形成され、完全に角質化して、赤みがかった点が点在する灰白色になります(唾液腺管の口)。
- カンジダ - 慢性カンジダ感染症が加わります。
- 毛様白板症はエプスタイン・バーウイルスによって引き起こされる病気です。
合併症とその結果
毛状白板症の不快な結果と合併症には、味覚の変化、カンジダ菌の感染による口腔粘膜の炎症(カンジダ性口内炎)、口内の不快感(チクチクする感じ、灼熱感)などがあります。
診断 毛髪性白板症
この疾患の診断は、臨床所見と臨床検査に基づいて行われます。組織学的検査では、上皮層の病変部に「毛羽立ち」が認められます。塗抹標本では、表層感染(カンジダ症)、粘膜の角質化、上皮の有棘層および顆粒層の肥厚と腫大、炎症が認められることがあります。
粘膜生検でエプスタイン・バーウイルス(EBV)が検出されます。HIV検査も行われ、Tヘルパーリンパ球の数も測定されます(白板症では正常範囲を下回ります)。EBVは、ポリメラーゼ連鎖反応(PCR)、免疫組織化学、電子顕微鏡検査、in situ ハイブリダイゼーション(ISH)など、様々な方法で検出できます。ISHは診断のゴールドスタンダードと考えられています。[ 8 ]
その他の方法としては、光診断スコープ(紫外線照射および組織発光の観察)を使用した機器検査、電子顕微鏡検査(電子流を誘導することにより、細胞内および微小分子レベルでの組織構造を研究する)、および光干渉断層撮影法の使用などがあります。
差動診断
鑑別診断としては、口腔カンジダ症、扁平苔癬、ヒトパピローマウイルスによる口腔粘膜内腫瘍、口腔扁平上皮癌などが挙げられます。ほとんどの場合、口腔毛状白板症は臨床的に診断可能であり、確定診断のための生検は必要ありません。
連絡先
処理 毛髪性白板症
毛状白板症は通常、特別な治療を必要とせず、HIV感染に伴う場合はHAARTで治癒することが多い。[ 9 ] 薬物療法は主にエプスタイン・バーウイルスの抑制を目的としている。また、特別な食事制限があり、辛いもの、熱いもの、塩辛いもの、酸っぱいものは食事から除外する必要がある。
口腔粘膜には特別なケア、具体的には消毒薬による洗浄が必要です。組織栄養を改善する局所製剤を使用し、全身強壮剤、生体刺激剤、そして必要に応じて鎮痛剤も使用します。
毛状白板症の治療は、患者の快適さを回復し、舌の正常な外観を回復し、他の口腔疾患を予防することを目的としています。[ 10 ]推奨される治療法には、手術、全身抗ウイルス療法、局所治療などがあります。
薬
ゲンチアナバイオレットは、1861年にシャルル・ロートによって「ヴィオレ・ド・パリ」という名称で合成されたトリフェニルメタン系染料です。1912年、チャーチマンは、クリスタルバイオレットがグラム陽性微生物に対してin vitroおよび動物モデルで殺菌作用を示すこと、また、いくつかのカンジダ属菌に対して抗真菌作用を示すことを実証しました。[ 11 ] それ以来、いくつかの研究でその抗菌・抗真菌作用が評価されています。
ゲンチアナバイオレットの抗ウイルス作用は、EBVウイルス産物が活性酸素種の形成を誘発し、ゲンチアナバイオレットが活性酸素種の強力な阻害剤であるという事実に基づいて調査されました。[ 12 ] クリスタルバイオレットは忍容性が高く、ヒトへの使用が承認されており、安価であることを考慮して、Bhandarkarらは[ 13 ]、HIV感染男性1名を対象に、毛状白板症の局所治療薬としてゲンチアナバイオレット(2%)を使用する研究を実施しました。ゲンチアナバイオレットは、1か月間、病変に3回局所塗布されました。1か月の追跡調査後、病気の完全な退縮が観察され、1年間の治療後も再発は観察されませんでした。
ポドフィリンは、ポドフィルム・ペルタタム(Podophyllum peltatum)の根茎と根から抽出された乾燥アルコール抽出物です。脂溶性物質で、細胞膜を透過して細胞複製を阻害します。局所化学療法剤として広く使用されています。[ 14 ] 安価で使いやすく、長期間にわたって効果を発揮します。
毛状白板症の局所療法として25%ポドフィリンアルコール溶液を使用した結果は、特に塗布後1週間で顕著である。症例シリーズでは、9人の患者がベンゾイン化合物のチンキ剤で25%ポドフィリンゾルで治療された。結果は、すべての病変の完全な退縮を示した。1週間以内に5人の患者、1週間後に2回目の塗布後に4人の患者が退縮した。これら4人の患者はより広範囲の病変を有していた。別の研究では、毛状白板症の男性患者6人が25%ポドフィリンを1日1回投与され、3〜5日ですべての病変の治癒が確認された。[ 15 ] Gowdyらは、舌に毛状白板症のあるHIV感染患者10人を評価し、片側に25%ポドフィリン樹脂溶液を1回局所塗布した。もう片側はコントロールとして使用した。患者は研究の2、7、30日後に評価された。患者は、味覚の軽度の変化、灼熱感、そして短期間の痛みを報告しました。特に塗布後2日目には、病変の退縮が見られました。
毛状白板症の局所療法で一般的に使用されるポドフィリンの投与量は 10 ~ 20 mg の範囲でした。
抗ウイルス療法には、アシクロビル、バラシクロビル、ファムシクロビルなどの薬剤が含まれます。デシクロビル、バラシクロビル、アシクロビル、ガンシクロビルなどの全身性抗ウイルス薬の投与を中止すると、毛状白板症の再発がよく観察されます。[ 16 ]
アシクロビルは、単純ヘルペスウイルスI型およびII型、EBウイルス、水痘帯状疱疹ウイルス、そしてサイトメガロウイルスに対して非常に効果的な化学療法用抗ウイルス剤です。アシクロビルクリーム外用剤を用いた唯一の研究は、Ficarraらによって実施されました[ 17 ]。著者らは、120人のHIV陽性患者のうち23人(19%)に毛状白板症を観察し、アシクロビルクリームの外用後、2人の患者で病状の完全治癒、1人の患者で部分的な退縮を認めました。
アシクロビル錠は、1日800mg(1錠中に200mg含有)を5回に分けて服用することを推奨します。2歳未満の小児には処方されません。妊娠中および授乳中の女性は、ベネフィット・リスク比を考慮し、慎重に使用する必要があります。副作用には、吐き気、下痢、倦怠感、かゆみ、発疹、頭痛、めまいなどがあります。貧血、黄疸、肝炎が現れることがあります。成分にアレルギーがある場合、腎不全または肝不全の患者、高齢者は服用量を減らす必要があります。
この病気が HIV 感染を背景に発症した場合は、逆転写酵素阻害剤(ジドブジン、ジダノシン)が使用されます。
カンジダ感染症は抗真菌薬(フルコナゾール、ケトコナゾール)で治療されます。
フルコナゾール - カプセル剤。治療初日に200~400mgを服用し、その後1~3週間かけて100~200mgを服用し、寛解状態が維持されます。この形態の小児には、カプセルを飲み込めるようになったら、通常5歳以降に投与できます。初期用量は1日6mg/kg、維持用量は3mg/kgです。
副作用としては、眠気、不眠、貧血、下痢、吐き気、頭痛、口渇、ビリルビン値の上昇、トランスアミナーゼ値などが考えられます。一部の薬剤(テルフェナジン、シサプリド、アステミゾールなど)との併用は禁忌です。
毛状白板症の治療では、局所角質溶解剤やレチノイン酸製剤も使用されます。
ビタミン
白板症の治療にはビタミン療法が適しています。酢酸トコフェロールとレチノールの油剤を経口投与します。飲み込む前に、しばらく口の中に含んでおきます。
レチノイドは、毛状白板症におけるランゲルハンス細胞の調節に関与する脱角化剤です。12例の患者に0.1%ビタミンAを1日2回局所塗布したところ、10日後に病変の退縮が認められました。[ 18 ] 22例の患者にトレチノイン溶液(レチンA)を15~20日間毎日塗布し、37例は未治療でした。治療を受けた患者の69%で病変の治癒が認められ、未治療患者の10.8%で自然退縮が認められました。[ 19 ] レチンAは高価な薬剤であり、長期使用により灼熱感を引き起こすことがあります。[ 20 ]
免疫力を高めるビタミンC、リボフラビンなどのビタミンB群が使われています。
理学療法治療
毛状白板症の治療プロトコルには理学療法が含まれます。これらの療法には、ジアテルモ凝固法と凍結療法があり、これらは角質増殖部を除去するために用いられます。
民間療法
民間療法としては、カモミールの花、菩提樹の花、セージなど、殺菌効果のある薬草の煎じ薬を使ったうがい薬を使うことができます。
外科的治療
切除術は毛状白板症の外科的治療法です。最も近代的な治療法はレーザーアブレーションで、レーザー光線を用いて粘膜表面から物質を除去し、蒸発させます。もう一つの治療法である凍結療法は、広く普及していません。
毛状白板症の外科的切除後3ヶ月間再発は認められなかった。しかし、ほとんどの患者は3ヶ月の観察期間後に新たな病変を発症した。[ 21 ]
このことを考慮し、手術と全身療法を比較すると、局所治療は全身的な副作用を引き起こさず、侵襲性が低く、長期間にわたって効果があるため、患者には局所治療を推奨すべきである。[ 22 ]
防止
この病気を予防する予防策は存在しない。
予測
半数の症例では、治療後に病状が安定します。同じ割合の症例で合併症(新たな病巣の出現)が発生します。エプスタイン・バーウイルス自体が消失するわけではなく、治療によってその増殖が抑制されるだけです。
毛状白板症自体は死に至ることはありませんが、免疫不全を背景にその症状が現れた場合は非常に警戒すべき兆候であり、平均余命(通常 1.5~2 年)の予後不良を示します。


