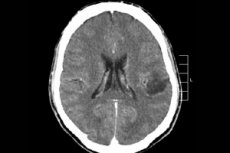
中枢神経系の多くの腫瘍プロセスの中で、脳神経膠腫が最も頻繁に診断されます - この用語は集合的であり、新生物はすべてのびまん性オリゴデンドログリアおよび星状細胞孔、星状細胞腫、星状芽細胞腫などを組み合わせています。このような腫瘍は、異なる程度の悪性腫瘍を持つことができ、グリア構造から形成されます - ニューロンの周りに局在する細胞。神経膠腫の位置の主な領域は、脳半球、脳室の壁とキアスマ - 視神経繊維の部分的な交差点の領域です。外部的には、腫瘍は、不明瞭な境界を持つ丸いまたは紡錘形の構成、ピンクがかった色または赤みがかった色合いの結節要素です。 [1]
疫学
約5%の症例では、神経膠腫は遺伝性の病理、特に神経線維腫症および支配的な遺伝を伴う他の症候群に関連しています。専門家は、脳神経膠腫の絶対大多数が散発的に発達すること、つまり明確な原因なしに発達することを指摘しています。
全体として、中枢神経系の主要な新生物は、すべての腫瘍の約2%、または人口10万人あたり21症例を超える症例を占めています。その中で、神経膠腫は症例の35〜36%で発生し、15%以上が膠芽腫です。
一部のデータによると、神経膠腫は女性よりも頻繁に男性に影響を与えます - 腫瘍は50歳以上の人の間で特に一般的です。
高齢者の間の神経膠腫の世界的な発生率は、ここ数十年で大幅に増加しています。この現象の理由はまだ確立されていません。
世界保健機関の定義によれば、組織学的特性が異なるグリア腫瘍の3つの主要なバリアントが特定されています。これらは、乏突起膠腫、星状細胞腫、および組み合わせた乏突起腺腫です。低悪性病理の各サブタイプの発生率は確実に決定されていません。いくつかの研究では、乏突起膠腫の発生率が5%から30%に増加し、星状細胞腫の発生率が減少していることが示されています。
グリア腫瘍は脳組織に浸透することができ、数年以内に低悪性度の病巣の大部分が悪性になります。 [2]
原因 脳神経膠腫
脳神経膠腫は腫瘍プロセスのグループ全体であり、その共通の特徴は、脳組織にあるCNSのグリア構造からの形成です。このような腫瘍は、高悪性および低悪性神経膠腫の2つの組織病理学的変異体に分けられます。
成長形成の原因は、脳ニューロンの構造的基礎と生存率を提供するニューログリア細胞(星状細胞、オリゴデンドロサイト)です。
グリア腫瘍のプロセスは、構造、遺伝子の変異の変化、攻撃性、臨床的特徴、診断特性、治療に対する反応、および患者の予後が大きく異なります。中枢神経系の胚および上部腫瘍性新生物、特に髄芽腫と上皮腫 - は組織構造が異なりますが、治療の点では類似しています。
グリア要素は、19世紀後半に神経系の別の構造カテゴリとして最初に分類されました。
神経組織は、栄養性、支持、保護、分泌の補助機能を持つ細胞で構成されています。ニューロンとグリオサイトは互いに存在し、それらは一緒に神経系を形成し、生物の重要な活動の一般的なプロセスで非常に重要です。
神経細胞は、星状細胞、乏突起膠細胞、上映細胞、およびミクログリアのいくつかの主要な形態に大まかに分類されています。
現在まで、科学者は神経症腫瘍形成の信頼できる原因に関する質問に答えることができません。おそらく、特定のマイナスの貢献は、放射性効果、感染症、中毒(特に化学、職業)によって行われます。遺伝性要因も重要です。
脳神経膠腫は、異常な成長と機能性につながる遺伝的欠陥を持つ異常な神経膠細胞から生じます - そのような構造は「未熟」と呼ばれます。不完全な細胞は、腫瘍が形成されている1つの領域に頻繁に配置されます。
簡単に言えば、グリアの形成は、修飾された神経細胞のカオスおよび散発的な成長の結果です。このプロセスは、表現腫細胞、乏突起膠細胞、星状細胞(星状細胞および未分化を含む星状細胞腫)から発達する可能性があります。 [3]
危険因子
専門家はグリア腫瘍病理学の形成の原因を正確に特徴付けることができないという事実にもかかわらず、場合によっては、主なリスク要因を排除することで外観を防ぐことができます。
- 電離放射線曝露には発がん性があり、白血病の発症と、若い年齢の人を含む密な構造で癌プロセスの形成を引き起こす可能性があります。頻繁で不合理な放射線医療処置である紫外線(ソラリウムを含む)も潜在的な発がん性効果に属し、脳を含むさまざまな臓器に腫瘍の出現を引き起こす可能性があります。
- 職業上の悪影響、中毒はしばしば癌性腫瘍の発症と因果関係があります。ゴムとガラス、農薬と燃料、金属と織物、塗料、実験室の試薬の生産は、特に危険だと考えられています。危険にさらされているのは、航空宇宙、石炭および金属産業、化学および副産物の製造プラント、建築材料と電極、燃料と潤滑剤、プラスチックとモノマーの労働者です。
- 大気、水、土壌汚染は、世界のすべての癌病理の最大4%の原因です。環境に大量に存在する発がん物質は、吸入空気、飲料水、食物で体に入ります。生態学的に安全でない地域に住む - 大規模な産業施設の近く、忙しい交通機関の交換 - は特に危険と見なされます。
- 感染性病理、特にウイルス感染症は、腫瘍の発生に有利な状態を生み出すこともあります。これを念頭に置いて、事前にワクチン接種され、感染性および寄生性疾患を防ぐことが重要です。
- タバコとアルコール中毒は、脳神経膠腫だけでなく、多くの種類の癌の危険因子と考えられています。
- 不十分な身体活動、過体重、不適切な栄養、代謝障害、頭部外傷、血管病理 - 細胞内障害の開始を引き起こす可能性のある追加のストレス因子。
- 高齢者は、体内の新生物の発達の最も一般的な期間であるため、55歳以上の人は自分の健康に特別な注意を払うべきです。
ただし、神経膠腫の発達の主なおよび最も重要な危険因子は、遺伝的素因のままです。
病因
現在まで、専門家は脳神経膠腫の発達に関する多くの仮定を持っています。それぞれの理論には独自の根拠がありますが、科学者がまだ特定していない唯一の正確で信頼できる病原性メカニズム。ほとんどの場合、新生物の発達における次の要因について話している:
臓器産卵の破壊と「間違った」細胞構造の形成で構成される胚形成の故障。
- 電離光線、化学物質の形での潜在的な発がん物質への曝露、食物添加物など。
- 頭部外傷;
- 世代から世代へと引き継がれた遺伝子障害(「家族性」神経膠腫);
- 免疫機能障害、神経感染。
ほとんどの神経膠腫には、周囲の正常な脳組織に浸透してびまんだ成長があります。悪性腫瘍の程度に応じて、腫瘍は症状なしに数年間発達する可能性があります。攻撃的なコースの場合、症状は数ヶ月で急速に増加します。
腫瘍形成の一部は、障害性変化によるものです。
脳幹はさまざまなレベルで影響を受ける可能性があります。びまん性脳幹神経膠腫は、解剖学的眼球学的および臨床的に異なります。そのような新生物、特に四肢麻痺プレートの神経膠腫 - は、進行の兆候がなく、比較的良性である可能性があります。一方、ポンチン神経膠腫は、その特定の悪性腫瘍、攻撃性、および予後不良によって特徴付けられます。
脳構造のびまん性病変は、大きな半球の3つ以上の解剖学的ゾーンが病理学的プロセスに関与しており、脳室周囲の発散とコーパスコール膠腫を通過する可能性があります。 [4]
脳膠腫は遺伝性ですか?
脳神経膠腫形成の十分に実証されたリスクは遺伝性です。つまり、直接祖先または同じ世代に類似または他の脳内腫瘍の存在です。放射性暴露と潜在的な発がん物質との定期的または長期にわたる接触は、状況を悪化させます。
神経膠腫を継承するだけでなく、局所化に関連することなく腫瘍の成長の増加を伴う病気も伴うことがあります。多くの場合、神経膠腫細胞では、特定の遺伝子または染色体の変化が検出されます。
ヒトの神経膠腫の発症に関連する主な病理は、テーブルにまとめられています。
|
病理学 |
染色体 |
遺伝子 |
さまざまな新生物 |
|
Li-Fraumeni症候群 |
17р13 |
TR53 |
神経胚葉新生物、星状細胞腫。 |
|
神経線維腫症 |
17Q11 |
NF1 |
視神経神経膠腫、症候性星状細胞腫、神経線維腫症 |
|
ターコット症候群 |
3p21、7p22 |
HMLH1、HPSM2 |
星状細胞腫 |
|
結節性硬化症(バーンビル症候群)。 |
9Q34、16p13 |
TSC1、TSC2 |
Gigantocellular下依存症星状細胞腫 |
グリア腫瘍の性質に関係なく、それが散発的な症例であろうと遺伝性病理であろうと、それは病理学的に変化した遺伝子の発現を伴う障害です。学習効果の結果として形成された新生物とは別に、他の状況では、遺伝的変化の原因は不明のままです。
症状 脳神経膠腫
局所症状の特徴は、脳神経膠腫の局在領域に直接依存し、あらゆる種類の内分泌障害、神経組織の圧迫、または局所破壊プロセスの結果になります。
新生物が頭頂帯にある場合、人は発作、感覚障害、聴覚障害などの症状に支配されます。
神経膠腫が支配的な半球の領域に局在する場合、言語障害、アグラフィア、アグノシアが検出されます。
側頭葉の新生物には、しばしば痙攣性発作、失語症、臭いの感覚障害と視覚機能、および呼吸困難が伴います。
頭蓋内圧が上昇すると、視野の制限、目の筋肉の麻痺、片麻痺とともに、対応する画像が発生します。
腫瘍プロセスの特異性のため、脳神経膠腫は常に神経学的症状を伴います。最初は顕著な一般的な衰弱があり、患者は絶えず眠りたい、働く能力が損なわれ、思考プロセスが遅くなります。この段階では、間違った診断を行い、その結果、間違った治療を処方するリスクが高くなります。他の非特異的症状の中で:
- 不安定な歩行、バランスの喪失(たとえば、自転車や登山の階段など)、手足のしびれなどを含む前庭障害。
- 視覚の緩やかな劣化、視覚像の倍増。
- 聴覚機能の劣化;
- 不明瞭なスピーチ;
- 食べ物や飲み物から独立した攻撃の形での吐き気と嘔吐。
- 模倣筋肉やその他の顔面筋の弱体化。
- 飲み込むときの不快感。
- 通常の頭痛(多くの場合、朝の時間に)。
臨床像は徐々に拡大して悪化します。一部の患者では、数週間以内に突然、文字通り「目の前」にゆっくりと起こります。後者の場合、私たちは脳の攻撃的で急速に発達している神経膠腫について話している。
最初の兆候
発達の初期段階における脳の神経膠腫には、顕著な症状はありません。最初の症状は、しばしば他の、それほど危険ではない病理の兆候と間違われます。
一般に、神経膠腫の臨床像は多様であり、病理学的焦点の位置とサイズによって決定されます。新生物が成長するにつれて、一般的な脳の症状が発生し、増加します。
- 標準的な薬物(非ステロイド性抗炎症薬)に反応しない持続的で正常な頭痛;
- 断続的な吐き気、時には嘔吐のポイントまで。
- 眼球エリアでの不快で重い感覚。
- 発作。
脳症状は、腫瘍が心室または液体に成長すると、特に激しいものです。脳脊髄液排水は損なわれ、頭蓋内圧が増加し、水頭症が発生します。このプロセスは、脳の特定の部分に影響を及ぼし、対応するクリニックの発達に影響します。
- 視覚機能には問題があります。
- 音声障害;
- 前庭障害(めまい、動きの協調障害)が発生します。
- 麻痺、腕の麻痺、脚。
- 記憶と濃度は損なわれています。
- 思考プロセスは損なわれています。
- 行動障害が出現しています。
初期段階では、症状は実質的に存在しません。または、注意が低いため、注目を集めません。このため、専門家は定期的な予防試験と検査に強くアドバイスすることです。結局のところ、腫瘍プロセスが早期に検出されるほど、治癒と生存の可能性が高くなります。 [5]
子供の脳の神経膠腫
小児期に見られる多くの脳腫瘍の中で、膠腫の割合は15〜25%の範囲です。子供は10代前半から20代前半で病気にかかることがありますが、3歳未満の赤ちゃんが病気にかかることは非常にまれです。
病理は、グリア細胞の突然変異の背景に反して始まります。現在までに、なぜこの突然変異が起こるのかという問題に対する答えはありません。
確実に学んだ唯一のことは、腫瘍成長のリスクの増加に関連する特定の遺伝性疾患が脳神経膠腫を発症する可能性を高めることです。
さらに、科学者は、グリア細胞が個々の遺伝子または染色体に発散する可能性があることを発見しました。この障害のため、突然変異メカニズムが始まりますが、これは遺伝性ではありません。これは、開発の最も初期の段階の1つで発生する可能性があります。
子供の歴史における急性白血病または網膜芽細胞腫の存在、または他の理由で脳照射が膠腫形成のリスクを大幅に増加させることは証明されています(一定期間後)。
小児期の症状は、病理学的焦点の悪性腫瘍の程度と局在に依存します。特定の症状と非特異的症状を区別します。
- 非特異的症状は、神経膠腫がある領域に「結ばれている」わけではありません。一般的な症状には、頭の痛み、めまい、食欲不振、食物摂取との関係なし、体重減少(不明な理由)、疲労感、学業成績の低下、集中障害、行動障害が含まれます。これらの兆候は、頭蓋内構造の圧縮によるものであり、成長腫瘤の直接圧力と脳脊髄液の循環における障害として説明できます。脳炭水化物のリスクがあります。
- 特定の症状は、グリア病理学的焦点の即時の位置に依存します。たとえば、小脳腫瘍には通常、子供の歩行障害とバランスが伴います。大きな脳の病変は、痙攣性発作と脊髄の腫瘍の成長 - 筋肉系の麻痺によって現れます。赤ちゃんの視力が急激に悪化したり、意識が乱れたり、睡眠が損なわれたり、他の発達上の問題が発生したりすることがあります。
原則として、小児期には、悪性神経膠腫は、その発達の数週間または数ヶ月でそれ自体を明らかにします。多くの場合、新生物の急速かつ制御されていない成長を特徴としています。
悪性グリア腫瘍の小児は、小児腫瘍学を専門とする小児臨床センターの医師によって治療されます。原則として、外科的治療、放射線、化学療法コースが使用されます。
最も重要な治療ステップは脳神経外科です。急進的であればあるほど、子供の治療の可能性は良くなります。しかし、外科的介入は必ずしも可能ではありません。特に、脳幹神経膠腫の除去や3歳未満の子供の放射線で問題が発生する可能性があります。
健康な組織に損傷を与えるリスクがあるため、中央脳(中脳および中脳)の神経膠腫は完全に除去することが困難です。腫瘍の完全な切除が不可能な場合、患者は緩和治療を処方されます。
悪性神経膠腫の子供は、厳密に制御された臨床試験を通じて決定された標準化されたプロトコルに従って治療されます。最も一般的なプロトコルは次のとおりです。
- HGG 2007をヒット:3〜17歳の子供の治療が含まれます。
- HIT SKK:乳児に適し(最大3歳)。放射線治療は含まれません。
神経膠腫の小児生存統計は、一般にあまり楽観的ではありません。ただし、特定の子供の治療措置の有効性を事前に予測することはできません。すべての医師の注文に注意深く従うことが重要です。これにより、回復の可能性が大幅に増加します。
フォーム
神経膠腫は、悪性と悪性が低く、激しい成長と転移の傾向があります。低悪性腫瘍は腫瘍の安全と同義ではないことを理解することが重要です。脳の新生物は、追加の体積を作り出し、脳構造を絞り、それがそれらの変位と頭蓋内圧の増加につながります。その結果、患者は死亡する可能性があります。
悪性星細胞腫には2つの主要なタイプがあります。これらは膠芽腫と未分化星状細胞腫であり、分子の変化に応じて細分化されています。星状細胞腫から発達し、悪性度が低い二次悪性腫瘍は、若い患者で最も頻繁に見られます。最初は悪性グリア型腫瘍が高齢患者でより頻繁に発生します。
構造的位置によっては、膠腫が入ってきます。
- 上腸骨(外側心室の領域の小脳の上に局在化する、大きな半球の局在);
- サブテントリアル(後頭蓋窩の小脳の下に局在する)。
組織学的特徴によれば、そのようなタイプの膠腫を区別します。
- 星状細胞神経膠腫が最も一般的です。次に、それは結節性とびまん性に細分化されます(後者は急速な成長と脳卒中パターンによって特徴付けられます)。
- 乏突起膠腫 - 患者の5%で発生します。石灰化の領域、ほとんどの場合、前頭葉にある石灰化の領域があります。
- 上肢神経膠腫 - 脊髄と心室の中央管の壁に並ぶ構造から成長します。多くの場合、脳の物質の厚さや脳の内腔に成長します。
下依存症、オリゴ域外腫などの混合病理学にも可能性があります。
すべての神経膠腫は、次の段階に分類されます。
- 明らかな臨床症状のない、ゆっくりと成長する比較的良性の新生物。
- 徐々に成長する「境界線」神経膠腫は、徐々にステージIII以降に変換されます。
- 悪性神経膠腫。
- 激しい攻撃的な成長と拡散を伴う悪性神経膠腫、予後不良。
悪性腫瘍の段階が低いほど、転移の可能性が低く、除去された新生物の再発性が低くなり、患者の治療の可能性が高くなります。最大の危険は、集中的な成長と発達を伴う低分化プロセスである多形性膠芽腫によってもたらされます。 [6]
神経膠腫の可能性のある最も一般的なバリアント:
- 脳幹と橋の病変を伴う神経膠腫は、脳が脊髄に接続する領域にあります。呼吸器、心臓、および運動機能の原因となる重要な神経因子が局所化されていることがあります。このゾーンが破損している場合、前庭と音声装置の作業が妨げられます。それはしばしば子供の頃に検出されます。
- 視覚神経膠腫は、視神経を取り巻く神経細胞に影響を与えます。病理は視覚障害と眼球症を引き起こします。子供の方が頻繁に発達します。
- 低悪性神経膠腫は、成長が遅いことを特徴とし、大きな半球と小脳に局在します。それは、若者(20歳前後の青少年や若年成人)でより頻繁に発生します。
- 脳梁の神経膠腫は、40歳から60歳までの個人の特徴であり、最も一般的に膠芽腫で表されます。
- キアスマの神経膠腫は光学接合ゾーンに局在するため、近視、視野損失、閉塞性油圧症、ニューロ内分泌障害を伴います。それはあらゆる年齢で発生する可能性がありますが、最も一般的には神経線維腫症の患者に影響します。
合併症とその結果
低悪性腫瘍の神経膠腫(グレードI-II、非常に悪性 - たとえば、星状細胞腫、オリゴ放射細胞腫、乏突起膠腫、多形性キサントローマ腫など)および高悪性腫瘍(グレードIII-IV-グレードII-IV-膠芽腫、麻酔腺腫、宇宙腫、オリゴストロマ、オリゴストロマ、オリゴストロマ。グレードIV神経膠腫は特に悪性です。
脳幹神経膠腫は、脳と手足の間の最も重要な神経のつながりが濃縮されるような脳領域に影響を与えるため、まさに非常に不利な予後があります。この領域のかなり小さな腫瘍でさえ、患者の状態を急速に劣化させ、麻痺を引き起こすのに十分です。
他の脳領域が影響を受ける場合、それほど不利な結果は発生しません。多くの場合、それは大脳皮質の腫瘍であり、治療にもかかわらず、患者の長寿命の機会を与えません。多くの場合、死を延期することだけが可能です。
医療統計によると、5年の生存率は多くの場合10〜20%しかありません。これらの数字は、悪性の程度と、実施された外科的介入の正確な局在と量の両方に大きく依存しています。病理学的焦点を完全に除去した後、生存率は大幅に増加します(時には - 最大50%)。治療の欠如またはその不可能性(何らかの理由で)は、患者の死につながることが保証されています。
低悪性グリア腫瘍の大部分は、脳組織に浸透し、数年にわたって悪性化することができます。
神経膠腫の再発のリスクは、専門家によって「非常に可能性が高い」と見なされます。それにもかかわらず、治療は無視されるべきではありません。可能な限り良好な生活の質を確保することが重要です。
再発性神経膠腫は、原発腫瘍よりも常に予後が悪い。しかし、治療最適化研究に基づく最新の治療プロトコルは、非常に悪性新生物の場合でも患者にとって十分に良い結果を達成することがよくあります。
化学療法後の可能な結果:
- 衰弱、衰弱、消化器疾患、口腔疾患;
- 中枢神経系の興奮性の増加、アセニア。
- 聴覚機能の劣化、耳鳴り、耳の鳴り響き。
- 発作、抑うつ障害;
- 高血圧の危機、血液パターンの変化。
- 腎不全;
- アレルギープロセス、脱毛、体の顔料の外観。
化学療法後、患者は免疫系の顕著な弱体化を指摘し、さまざまな感染性病理の発達を引き起こす可能性があります。
診断 脳神経膠腫
脳神経膠腫は、次の兆候によって疑われる可能性があります。
- 患者には、新生物の皮質位置とその遅い発達の特徴である局所的または全身性発作があります。エピオン発生は、低悪性度のグリア腫瘍の患者の80%と高悪性度の膠腫患者の30%に見られます。
- 頭蓋内圧の増加は、右前頭および頭頂葉に位置する質量の特徴です。血液循環と液体循環の高い頭蓋内圧障害に関連することは、一定の頭痛、嘔吐、視覚障害、眠気の吐き気の増加の出現を伴います。視神経の浮腫、流用神経の麻痺があります。頭蓋内圧力が重要な価値に増加すると、com睡状態と死の発達につながる可能性があります。 IOPのもう1つの原因は、水頭症です。
- 患者は焦点視を成長させています。上層の形成では、運動球と感覚球が乱れ、ヘミオピア、失語症、認知障害が進行します。
医師が脳の新生物の存在を疑う場合、造影剤(ガドリニウム)の導入なしにMRIを実行して、その場所、サイズ、および追加の特性を調べることが最適です。磁気共鳴画像法が不可能な場合、コンピューター断層撮影が行われ、磁気共鳴分光法が分化の方法として使用されます。これらの診断方法の情報にもかかわらず、最終診断は腫瘍の焦点の切除中の組織学的確認後にのみ行われます。
上記の基準を考えると、徹底的な歴史、ソマト神経学的状態の評価、および機能状態で診断を開始することをお勧めします。神経学的状態は、考えられる知的障害およびmnest障害の決定とともに評価されます。
推奨される臨床検査:
- 本格的な一般的な臨床血液検査。
- 全血化学パネル。
- 尿検査;
- 血液凝固研究;
- 腫瘍マーカーの分析(AFP、ベータ-HCG、LDH-松果体ゾーンの病変が疑われる場合は関連)。
膠芽腫および未分化星状細胞腫の患者の予後ポイントを明確にするために、IDH1 | 2-1遺伝子変異とMGMT遺伝子メチル化が評価されます。乏突起膠腫および乏膠散化腫の患者では、1p | 19Qコドレレーションが決定されます。
まず第一に、機器の診断は、脳の義務的な磁気共鳴画像法(時には - 脊髄)によって表されます。 MRIは、標準のT1-2、Flair、ContrastのT1モードを使用して3つの投影で実行されます。
示されている場合、血管ネットワークの超音波、運動および音声セクションの機能的磁気共鳴画像法、血管造影、分光法、MRトラクトグラフィー、灌流が行われます。
追加の調査には以下が含まれます。
- 脳の脳波;
- 神経外科医、腫瘍医、放射線科医、眼科医、放射線科医との協議。
差動診断
鑑別診断は、非腫瘍の病理、特に動脈毒または動脈奇形によって引き起こされる出血、および偽腫瘍の脱髄プロセス、炎症性疾患(トキソプラズモ症、脳膿瘍など)で必然的に行われます。
さらに、原発腫瘍の焦点と中枢神経系の転移を区別します。
最新の磁気共鳴画像機能により、CNSの主要な焦点の起源を見つけるのに十分なほど正確に診断測定を実行することができます。脳のMRIは、コントラストの有無にかかわらず、T1、T2フレアモード - 3つの投影、または軸方向投影(SPGRモード)の薄いスライスで実行されます。これらの診断方法により、新生物の位置、サイズ、構造的特性、血管ネットワークおよび近くの脳領域との関係を正確に決定できます。
さらに、CT(コントラストの有無にかかわらず)、CT血管造影(MR血管造影)、MRトラクトグラフィー、MR、またはCT灌流は、鑑別診断の一部として実施される場合があります。メチオニン、コリン、チロシン、およびその他のアミノ酸を含む脳のCT/PETは、示されたときに使用されます。
処理 脳神経膠腫
特定の療法は、外科的、化学療法、放射線測定で構成されています。可能であれば、腫瘍の焦点を完全に切除することは必須です。これにより、診断の迅速な症状の緩和と組織学的確認が可能になります。
照射は、患者の平均余命の増加にプラスの効果をもたらします。 1.8-2 Gyの個々の照射用量に分割された58〜60 Gyの総投与量が標準として投与されます。腫瘍は局所的に照射され、さらにその周りで最大3 cmを捕獲します。放射線療法は、黒球療法とは対照的に、より受け入れられます。場合によっては、ガンマナイフまたは線形ガスペダルを照射することと、中性子飼育ホウ素療法で構成される放射線外科手法が推奨されます。
補助化学療法の必要性は議論の余地があります。場合によっては、ニトロソウレアの準備により、患者の平均寿命を最大1年半増加させることができましたが、そのような化学層を使用した結果は陰性でした。今日、細胞毒性剤、ネオアジュバント療法(放射線前)、組み合わせた薬物、動脈内化学療法、またはさらなる幹細胞移植を伴う高用量化学療法が積極的に使用されています。
一般に、神経膠腫の治療を成功させるためには、包括的なアプローチが非常に重要であり、その程度は質量の悪性腫瘍、そのサイズ、患者の一般的な健康状態に依存します。
脳幹神経膠腫に関連して、外科的介入はめったに使用されません。手術の主な禁忌は、焦点の局在化の領域です - 重要な部分に近接しています。場合によっては、術前および術後化学療法を使用して、顕微手術方法を使用して体幹の神経膠腫を除去することが可能です。このような介入は非常に複雑であり、脳神経外科医の特別な資格が必要です。
放射線手術、特に、高イオン化用量にさらされた立体手術は非常に効果的です。新生物の発達の初期段階でそのような技術を使用することで、長期にわたる寛解や患者の完全な治療を達成することができる場合があります。
放射線は多くの場合、化学療法と組み合わされ、介入の有効性を改善し、放射線負担を軽減します。神経膠腫では、すべての化学予防剤が治療的に成功しているわけではないため、個別に処方され、必要に応じて処方が調整されます。
主な治療に関係なく、痛みを軽減し、頭蓋内圧を下げるために、症候性療法が処方されます。特に、コルチコステロイド薬、鎮痛薬、鎮静剤。
薬
コルチコステロイド薬は腫れに影響を及ぼし、数日間の神経症状の重症度を減らします。ただし、複数の副作用と化学療法薬との不利な相互作用の可能性の増加により、ステロイドの最小限の用量が使用され、できるだけ早くそれらを中止します(たとえば、手術後)。
抗けいれん薬は、すでにてんかん発作を経験した患者の二次予防尺度として体系的に使用されます。これらの薬は、深刻な有害症状を引き起こし、化学療法薬とも相互作用する可能性があります。
神経膠腫における血栓障害形成のリスクが非常に高い(最大25%)ため、抗凝固剤は術後段階で特に関連しています。
抗うつ薬酸症を服用することから良い効果が予想されます。メチルフェニデートを2回の用量で10〜30 mg/日使用することで、多くの場合、認知能力を最適化し、生活の質を向上させ、作業能力を維持できます。
|
神経学的失敗と脳浮腫の兆候(頭の痛み、意識の乱れ)は、コルチコステロイド薬、特にプレドニゾロンまたはデキサメタゾンによって排除されます。 |
|
コルチコステロイドのスキームと投与量は、最小有効用量の実践とともに個別に選択されます。治療コースの終わりに、薬物は徐々に撤回されます。 |
|
コルチコステロイドは、胃保護薬と一緒に摂取されます - プロトンポンプブロッカーまたはH2-ヒスタミンブロッカー。 |
|
利尿薬(フロセミド、マンニトール)は、コルチコステロイド薬の補助として、脳構造の重度の腫れと変位に処方されています。 |
|
痙攣性発作(ANAMNESISを含む)または脳波のてんかん型症状の場合、抗けいれん療法がさらに処方されます。抗けいれん薬は予防目的で処方されていません。 |
|
化学療法の適応患者は、肝臓酵素機能に影響を与えない抗けいれん薬を服用することをお勧めします。選択した薬:ラモトリギン、バルプロ酸、レベチラセタム。使用しないでください:カルバマゼピン、フェノバルビタール。 |
|
脳神経膠腫の頭の痛みは、コルチコステロイド治療で管理されています。 |
|
頭痛の場合には、非ステロイド性抗炎症薬またはトラマドールが使用される場合があります。 |
|
患者が非ステロイド性抗炎症薬を服用している場合、手術中の出血の可能性を最小限に抑えるために、手術の数日前に中止されます。 |
|
選択された痛みの場合、フェンタニルやトリメペリジンなどの麻薬鎮痛薬が推奨される場合があります。 |
|
術後3日目から肺塞栓症を防ぐために、低分子量ヘパリン、特にエノキサパリンナトリウムまたはナドロパリンカルシウムの投与が処方されます。 |
|
患者が体系的な抗凝固剤または抗凝固療法を受けている場合、手術の前にさらに離脱し、手術の24〜48時間後に再開する前に、外科的介入の1週間前に低分子量ヘパリンに移されます。 |
|
神経膠腫の患者が下肢の静脈血栓症を患っている場合、直接抗凝固剤による治療が行われます。カバフィルターを配置する可能性は除外されていません。 |
脳の悪性神経膠腫に対する化学療法
神経膠腫の基本的な抗腫瘍化学療法レジメンは、次のと考えられています。
- 1日目にロムスチン100 mg/m²、1日と8日目にビンクリスチン1.5 mg/m²、8日目から21日目まで70 mg/mg、6週間ごとにコース。
- 6週間ごとにロムスチン110 mg/m²。
- テモゾロミド5/23 150〜200 mg/m²から5日目から5日目、28日ごとに。
- 化学放射線治療の一部としてのテモゾロミド、放射線が与えられる毎日75 mg/m²。
- 4週間ごとに1日目から5日目に、シスプラチンまたはカルボプラチン(80 mg/m²)およびテモゾロミド150-200 mg/m²を含むテモゾロミド。
- コースの1〜8日目と15〜22日目に100 mg/m²のテモゾロミド7/7、4週間ごとに繰り返されます。
- ベバシズマブは1日目と15日目に5〜10 mg/kg、1日目と15日にイリノテカン200 mg/m²、4週間ごとに繰り返されます。
- ベバシズマブは、1日目、15日、29日、およびロムスチン90 mg/m²で6週間ごとに90 mg/m²に5〜10 mg/kgを使用します。
- ベバシズマブは1日目と15日目に5〜10 mg/kg、1日、8、15、22日目にロムスチン40 mg、6週間ごとに繰り返されます。
- ベバシズマブは1日目と15日に5〜10 mg/kg、4週間ごとに繰り返されます。
多くの場合、細胞質薬は腫瘍細胞の成長をうまく阻害しますが、健康な組織や臓器に対する選択性は示されません。したがって、専門家は、神経膠腫の化学療法が不可能である多くの禁忌を特定しています。
- 化学予防剤に対する過度の個々の感受性。
- 心臓、腎、肝機能の代償不全。
- 骨髄における落ち込んだ造血;
- 副腎機能の問題。
化学療法は非常に注意して投与されます:
- 重大な心臓リズム障害のある患者;
- 糖尿病で;
- 急性ウイルス感染の場合;
- 高齢患者に;
- 慢性アルコール依存症(慢性アルコール中毒)に苦しむ患者。
化学予防薬の最も深刻な副作用は毒性です。細胞症は血液細胞の機能を選択的に妨害し、組成を変化させます。結果として、血小板および赤血球の腫瘤は減少し、貧血が発生します。
患者に化学療法のコースを処方する前に、医師は常に薬物の毒性の程度と使用後の合併症の可能性を考慮します。化学療法コースは、専門家と定期的な血液監視によって常に慎重に監視されています。
細胞質療法の可能性のある結果:
- ガントネス、衰弱;
- 食物を飲み込む困難、乾燥粘膜、歯周炎、消化不良。
- 中枢神経系の不安定性、man病障害、発作症候群、アステニア。
- 聴覚機能の劣化;
- 高血圧危機の発達まで血圧の上昇。
- 血小板、赤血球、白血球、複数出血、内部出血の減少。
- 腎不全;
- アレルギープロセス;
- 脱毛、色素沈着の増加の領域の出現。
化学療法のコースの後、患者は感染症を発症するリスクが高く、筋肉と関節の痛みが一般的です。
失敗後の療法後の有害な効果のリスクを減らすために、さらなるリハビリテーション対策が必然的に処方されます。その目的は、正常な血液数、心血管活動の安定化、神経学的状態の正常化を回復することです。十分な心理的サポートが必然的に実践されています。
外科的治療
手術は、腫瘍の焦点を可能な限り除去するために行われ、頭蓋内圧を低下させ、神経学的不足を軽減し、研究に必要な生体材料を提供するはずです。
- この手術は、専門家が神経腫瘍学的介入を経験している専門の脳神経外科部門または診療所で行われます。
- 外科医は、神経膠腫の局在化が疑われる領域でプラスチック骨のトレパネーションによるアクセスを実行します。
- 新生物が解剖学的に運動領域または経路に近い位置に位置する場合、または核または頭蓋神経に沿って、術中の神経生理学的モニタリングが使用されます。
- ニューロナビゲーションシステム、5-アミノレブレン酸による術中蛍光ナビゲーションは、新生物の除去を最大化するために望ましい。
- 介入後、コントロールCTまたはMRI(コントラスト注入の有無にかかわらず)が1日目に行われます。
|
神経膠腫の外科的切除が不可能であるか、最初に不足していると認識されている場合、または中枢神経系のリンパ腫が疑われる場合、生検(オープン、ステレオテクティック、ナビゲーション監視など)が行われます。 |
|
治療的戦術は組織学的像に大きく依存するため、脳膠腫症の患者は立体生検によって検証されています。 |
|
特定の状況では、高齢患者では、重度の神経障害の場合、幹やその他の重要な部分の神経膠腫の局在化の場合に、一般的な医療相談後の症状とイメージング情報に基づいて治療が計画されています。 |
|
毛様体星状細胞腫の患者、および脳幹新生物の結節形態と外植物プロセスの患者は、切除または開いた生検を受けるために推奨されます。 |
|
びまん性ポンチン神経膠腫およびトランクの他のびまん性新生物の患者は、放射線および抗腫瘍薬療法で治療されます。そのような場合、検証は必要ありません。 |
|
四肢麻痺板神経膠腫の患者は、脳炭水化物の除去後に体系的な磁気共鳴と臨床モニタリングを受けます。新生物が成長の兆候を示している場合、さらなる照射で除去されます。 |
|
低悪性度の悪性神経膠腫の部分切除または生検を実施する場合、2つ以上の危険因子を持つ患者は、必然的に放射線および/または化学療法で治療されます。 |
|
総切除は、下依存症の巨大細胞星状細胞腫患者に必須です。 |
|
Everolimusは、びまん性下依存症の巨大細胞星状細胞腫に処方されています。 |
|
腫瘍組織の根治的切除の品質を明確にするために、介入後に磁気共鳴画像法で粉砕星状細胞腫を除去する必要があります。 |
|
膠芽腫では、術後療法をテモゾロミド投与と組み合わせる必要があります。 |
|
手術後の未分化星状細胞腫では、さらなる薬物療法による放射線療法が示されています。ロムスチン、テモゾロミドが使用されます。 |
|
未分化の乏突起膠腫または乏突起球腫の患者は、手術後に放射線と化学療法(テモゾロミドまたはPCV単剤療法)の両方を投与されます。 |
|
広範囲の悪性神経膠腫の高齢患者は、低拡張モードで照射されるか、テモゾロミドによる単剤療法が実施されます。 |
|
神経膠腫の再発の場合、再手術とその後の治療戦術の可能性は、専門家のコンセリウムによって議論されています。再発のための最適なレジメン:再手術 +全身化学療法 +繰り返し放射線曝露 +緩和測定。再発性腫瘍成長の局所的な軽微な領域がある場合、放射線手術が使用される場合があります。 |
|
再発性神経膠腫の成長に最適な薬物は、テモゾロミドとベバシズマブです。 |
|
非常に悪性の乏突起膠腫と未分化星状細胞腫の再発は、テモゾロミド治療の兆候です。 |
|
多形性中canthoaStoSocytomaは、必須のアジュバント化学療法なしで除去されます。 |
神経膠腫の特異性の1つは、それらの治療と除去の困難です。外科医は、腫瘍の組織を可能な限り完全に除去し、状態の補償を達成することを目指しています。多くの患者は生活の質を向上させ、それを延長することができますが、非常に悪性腫瘍の場合、予後は不利なままです。病理学的焦点の再成長の可能性が高まっています。
脳の神経膠腫の栄養
悪性腫瘍の患者の食事 - 残念ながら、多くの人があまり注意を払っていない重要なポイント。一方、食事の変化のおかげで、神経膠腫の発症を遅らせ、免疫を強化して揺さぶることが可能です。
食事の変化の主要な領域:
- 代謝プロセスの正常化、免疫保護の強化。
- 身体の解毒;
- エネルギー電位の最適化;
- そのような困難な時期に、すべての臓器と身体のシステムの正常な機能を確保します。
低悪性新生物の初期段階の患者と膠芽腫の最後の段階の患者として、合理的でバランスの取れた食事が必要です。慎重に選択された食事は、一般的な幸福、損傷した組織の回復の改善に貢献します。これは、細胞症および放射線治療の背景に対して特に重要です。栄養成分のバランスと適切な代謝プロセスは、感染性病巣の形成、炎症反応をブロックし、身体の疲労を防ぎます。
脳膠腫には、以下の食品と飲み物が推奨されます。
- 赤、黄色、オレンジ色の果物と野菜(トマト、桃、アプリコット、ニンジン、ビート、柑橘類、柑橘類)を含むカロテノイドを含む、放射線療法の悪影響から健康な細胞を保護します。
- キャベツ(カリフラワー、ブロッコリー、芽キャベツ)、大根、マスタード、およびインドールを含むその他の植物製品 - 有害な毒性および化学因子を中和する活性物質。
- グリーンズ(ディル、パセリ、若いタンポポとイラクサの葉、ルバーブ、ルッコラ、ほうれん草)、グリーンエンドウ豆とアスパラガス、アスパラガス豆、および藻類(海藻、スピルリナ、クロレラ);
- 緑茶;
- ニンニク、タマネギ、パイナップル、抗腫瘍と解毒能力を備えたパイナップル。
- ブラン、シリアル、全粒パン、マメ科植物、穀物、種の芽が出る。
- 暗いブドウ、ラズベリー、イチゴとイチゴ、ブルーベリー、ブラックベリー、ザクロ、スグリ、ブラックカラント、ローワンベリー、ブルーベリー、海の馬車、チェリー、その他のベリーは、フリーラジカル、ウイルス、カルシン剤
- 低脂肪乳製品。
消化器系と全身に重い脂肪の多い食品を負担してはなりません。絞りたての自家製ジュース、スムージー、一口を使用すると便利です。魚油、亜麻仁油、亜麻の種子などのオメガ3脂肪酸の供給源を皿に追加する必要があります。
砂糖やお菓子を完全に避ける方が良いです。しかし、一杯の水を含むスプーン一杯の蜂蜜は傷つきません。ミツバチ製品には、抗炎症、抗酸化、抗腫瘍効果が顕著になります。蜂蜜の使用に対する唯一の禁忌は、製品に対するアレルギーです。
食事から除外する必要があります。
- 肉、ラード、オファル;
- バター、脂肪乳製品;
- スモーク肉、ソーセージ、缶詰の肉、魚。
- あらゆる形のアルコール;
- お菓子、ペストリー、ケーキ、ペストリー、キャンディー、チョコレート。
- 便利な食べ物、ファーストフード、スナック。
- 揚げ物。
毎日、十分な野菜、緑、果物、きれいな飲料水を消費する必要があります。
化学療法中としばらくの間、自家製の野菜とフルーツジュースを飲み、自家製の低脂肪カッテージチーズ、ミルク、チーズを食べる必要があります。たくさんの液体を飲み、歯を磨き、口を頻繁にすすぐことが重要です(1日約4回)。
脳神経膠腫患者の最適な食事:
- 野菜のキャセロール;
- 穀物で作られたサイドディッシュとスープ(できればそば、オートミール、米、クスクス、ブルガー);
- 蒸しチーズケーキ、プリン、キャセロール。
- 煮込み野菜と焼き野菜。
- シチュー、野菜スープ、マメ科植物(大豆を含む)、パテ、スフレの1枚目と2番目の料理。
- スムージー、緑茶、コンポット、一口。
防止
人が健康的なライフスタイルをリードし、彼の親relativeの中で癌の病理の症例がなかった場合、彼は脳膠腫を取得しないすべての機会を持っています。そのような腫瘍の特定の予防はないため、主な予防ポイントは、適切な栄養、身体活動、悪い習慣の回避、職業および家庭の危険の欠如と見なされます。
専門家は、多くのシンプルでありながら効果的な推奨事項を提供します。
- より多くの純粋な水を飲み、甘くしたソーダ、包装されたジュース、エネルギー飲料、アルコールを避けてください。
- 職業および家庭の危険を避けてください:化学物質との接触、腐食性溶液、液体。
- 沸騰、煮込み、ベーキング、揚げ物で食べ物を準備してみてください。健康で高品質の自家製食品を好みます。
- あなたの食事の大部分は、時期に関係なく、グリーンを含む植物食品でなければなりません。
- 別の否定的な要因は太りすぎであり、それを取り除く必要があります。体重制御は、全身の健康にとって非常に重要です。
- 植物油は、バターとラードよりも常に好まれる必要があります。
- 可能であれば、環境に優しい製品、ホルモンのない肉、硝酸塩や農薬のない果物、果物を好むことが望ましいです。赤身の肉を完全に避ける方が良いです。
- マルチビタミン製剤を適応と大量に服用しないでください。医師の処方箋なしでは薬を服用しないでください。自己メディケーションは非常に非常に危険です。
- 疑わしい症状が現れた場合、状況の悪化、悪影響、合併症の発症を待つことなく、医師を訪問する必要があります。
- 高血糖指数を持つお菓子と食品は、食事の望ましくない成分です。
- 人が医師に行くほど、治癒の可能性が良くなります(これは、脳の神経膠腫を含むほとんどすべての病気に当てはまります)。
腫瘍病理学の形成を防ぐために、睡眠と休息に十分な時間が必要です。アルコール飲料の過度の消費を避け、高品質の自然食品を好み、ガジェット(特に携帯電話)の使用を減らします。
腫瘍疾患は、高齢者や老人でしばしば発生します。したがって、幼い頃からあなた自身の健康を監視し、不健康なライフスタイルと不健康な習慣によって病理学的プロセスを誘発することではないことが重要です。
腫瘍学の正確な根本原因はまだ明らかにされていません。しかし、もちろん、特定の役割は、不利な職業的および環境条件、イオン化および電磁放射への曝露、ホルモンの変化を果たします。太陽の下で定期的に滞在しないでください。周囲温度の突然の変化、お風呂やサウナの過熱、しばしば熱いお風呂やシャワーを浴びます。
別の質問:治療が成功した後、脳神経膠腫の再発を防ぐ方法は?新生物の成長の再発は複雑であり、残念ながら頻繁な合併症であり、事前に予測することは困難です。患者は、定期的な予防試験と検査を受け、腫瘍医を訪問し、少なくとも年に2回、医師を訪問し、健康的なライフスタイルをリードし、健康的で自然な食品を食べ、中程度の身体活動を実践することをお勧めします。別の条件は、人生への愛、健康的な楽観主義、いずれの状況でも成功に対する前向きな姿勢です。これには、家族や職場での友好的な雰囲気、忍耐と近親者からの無条件のサポートも含まれます。
予測
脳の状態とその検出時の神経膠腫の特性は、治療が投与したのと同じくらい生存率に影響します。患者の満足のいく一般的な健康と彼の年齢は予後を改善します(予後は若い患者でより楽観的です)。重要な指標は、新生物の組織学的像です。したがって、低悪性度の膠腫は、未分化神経膠腫よりも予後が優れており、さらに膠芽腫(最も不利な腫瘍プロセス)があります。星状細胞腫は、乏突起膠腫よりも予後が悪い。
悪性星細胞腫は治療に対する反応が不十分であり、6〜5年の生存率が比較的低いです。同時に、低悪性度膠腫の平均寿命は1〜10年と推定されます。
悪性星細胞腫は本質的に不治です。治療の方向には、通常、神経学的症状(認知機能障害を含む)を減らし、生活の質を維持しながら平均余命を増やすことが含まれます。症候性療法は、リハビリテーション対策の背景に惹かれます。心理学者の仕事も重要です。
過去10年間、科学者は脳腫瘍の性質とそれらの治療方法を理解することにある程度進歩してきました。病気の予後を最適化するために、さらに多くのことをすべきです。今日の専門家の主なタスクは次のとおりです。脳神経膠腫には、発達の初期段階とその後の段階で、問題を効果的に排除するためのいくつかのスキームが必要です。


