新しい出版物
消化管(食道および胃)運動障害(アカラシア、胃不全麻痺、嚥下障害など)は、人口の20%以上に影響を与え、深刻な罹患率と費用を伴います。薬物療法、行動介入、手術といった標準的な治療法は、効果が限られていることが多く、蠕動運動の協調を回復させることはできません。
- 既存のデバイスが問題を解決できない理由。消化管への電気刺激は1960年代から研究されてきましたが、臨床的に承認されているインプラント(例:胃不全麻痺用のEnterra、肥満治療用のVBLOC迷走神経刺激装置、便失禁治療用のInterStim仙骨刺激装置)は主にオープンループで動作し、胃内容排出に対する効果が不安定になることがよくあります。その理由は、一定パラメータを持つ1つまたは複数の電流源では、自然な蠕動運動の時空間的な複雑さを再現できないためです。
- 「模倣」されるべき生理学。蠕動運動は閉ループであり、感覚信号(伸張、温度、化学刺激)→筋層間神経叢および平滑筋における反射反応という経路を辿ります。食物輸送に加えて、蠕動運動は腸管脳求心性シグナルと満腹ホルモン(GLP-1、インスリン、グレリン)に影響を与え、食欲と満腹感を形成します。運動障害では、これらのループが破綻します。
- 技術ギャップ。「正しい」波を再現するには、筋層間神経叢と筋層付近への多チャンネル刺激が必要です。しかし、そこへのアクセスには通常、侵襲的な手術が必要です。高度な内視鏡技術(NOTESなど)は複雑で、広く普及していません。粘膜下層に電極を正確に配置し、「センシング→刺激」の閉ループで動作できる低侵襲性の機器が必要です。
- 新たな研究がもたらすもの。著者らは、内視鏡を用いて設置される、電気刺激と化学刺激を併用したマルチチャンネル神経補綴装置について述べている。この補綴装置は、食塊の通過に関する信号に基づいて協調蠕動波を誘発することができ、運動能力を回復させるだけでなく、代謝反応を調節し(「摂食」状態に近づける)、目的の層へのアクセス、時空間的な協調、そして閉ループにおける動作といった重要なギャップを埋める。
要するに、広範囲に及ぶにもかかわらず、適切に治療されていない食欲不振という、臨床的に大きなニッチ領域が存在するのです。従来の「オープン」な刺激薬は、自然な生理機能を模倣していません。したがって、インプラントに「消化管のように考える」ように、つまり、食塊を感知し、自然な信号が通過するまさにその場所、つまり筋層間神経叢で生理的な蠕動運動を誘発するように教えることは理にかなっています。
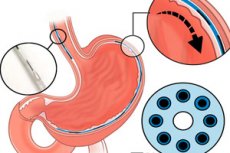
MIT、ハーバード大学、ブリガム大学の研究チームは、食物塊を「閉ループ」で感知し、協調的な蠕動運動を誘発する小型の食道・胃インプラントを開発しました。豚の実験では、このデバイスは食道と胃の運動機能を回復させただけでなく、食後(摂食後)の状態に類似したホルモン変化も誘発しました。インプラントは内視鏡を用いて設置され、開腹手術は不要です。この研究はNature誌に掲載されました。
彼らは何を思いついたのでしょうか?
- インプラント本体。直径約1.25mmの細い「繊維状」神経プロテーゼで、1cmごとに7個の電極と、局所的な物質送達(電気刺激および化学刺激)のためのマイクロチャネルを備えています。その柔軟性と寸法により、内視鏡の標準的な器具用チャネル(2.8~3.2mm)から挿入可能です。
- 設置。内視鏡器具が開発されました。ニチノール製の「フック」を逆方向に引っ張る針、ハイドロダイセクション、そして重要なポイントである組織インピーダンスによる粘膜下層の探索により、筋層直上、腸間膜神経叢付近に正確に配置します。
- 閉ループ。システムはボーラス信号(筋電図/腔内センサー)を読み取り、刺激パターンを選択することで、自然な蠕動運動に類似した連続的な収縮を誘発します。「興奮性」刺激と「抑制性」刺激を組み合わせたり、微量薬物投与によって括約筋を局所的に弛緩させたりすることも可能です。
動物に示されたもの
- 食道: インプラントは、実際に飲み込むことなく「嚥下波」を発生させました。これには、下部食道括約筋の制御された弛緩 (グルカゴンの微量送達による) と、プログラム可能な前進/後退波 (基本的には蠕動「ジョイスティック」) が含まれます。
- 胃。刺激20分後、蠕動運動の頻度は対照群と比較して約2倍に増加した(n≈4、p<0.05)。
- 代謝による「満腹感の錯覚」。空腹状態では、30分間の刺激(食道または胃)がホルモンの変化を引き起こし、GLP-1とインスリンの増加、グレリン(食欲ホルモン)の減少が見られました。胃の刺激では、グルカゴンの増加も観察されました。全体的なプロファイルは食後の状態に類似していました。
安全性とエンジニアリングの詳細
短時間のin vitro生体適合性試験(材料抽出物)では毒性は認められませんでした。in vivoでは、移植後7日目で壁の伸展性は正常で、デバイスの移動や組織損傷は認められませんでした。(耐久性と信頼性をさらに高めるには、長期試験が必要です。)
なぜこれが必要なのでしょうか?
- 運動障害および難治性疾患。アカラシア、胃不全麻痺、嚥下障害、術後障害など、従来の薬剤や手術では効果が不十分な場合が多い疾患。局所マルチチャンネル刺激は、既存の「シングルチャンネル」オープンループインプラントよりも、より現実の生理機能に近い刺激を提供します。
- 代謝障害。腸管脳求心性神経経路を制御することで、このデバイスは食欲と代謝を調節する可能性があり、これは肥満や糖尿病の診断に興味深いものです(今のところ仮説であり、ヒトにおける証拠はありません)。
限界と今後の展望
これは豚を用いた急性期・亜急性期の前臨床研究です。今後は、接触安定性、エネルギー供給、線維化リスク、精密刺激プロトコルに関する長期研究、そして重度の運動障害患者を対象とした初期臨床試験が予定されています。しかし、既に蠕動運動を指示通りに「オン」にし、ホルモン反応を満腹感へと誘導できることが示されています。しかも、これらはすべて内視鏡的アクセスによって実現可能です。

