新しい出版物
前立腺がんを免疫療法で治療することは現在困難です。しかし、米国最大級のがん研究・治療機関の一つであるCity of Hope®の研究者らが開発したキメラ抗原受容体(CAR)T細胞療法を用いた世界初の第1相臨床試験の結果は、前立腺がん患者が細胞免疫療法によって安全に治療でき、有望な治療効果が得られることを示しています。この第1相臨床試験の結果は、本日Nature Medicine誌に掲載されました。
この研究では、前立腺幹細胞抗原(PSCA)が前立腺を越えて転移し、ホルモン療法に反応しなくなった転移性去勢抵抗性前立腺がん(mCRPC)の患者14名をCAR-T細胞療法で治療しました。米国では、このタイプの前立腺がんを患う男性が毎年34,000人以上亡くなっています。
シティ・オブ・ホープ大学血液学・造血細胞移植科の助教授、ソール・プライズマン博士らは、前立腺がん患者で高発現していることが分かっている前立腺幹細胞抗原(PSCA)と呼ばれるタンパク質を標的とするCAR-T細胞を開発しました。この治療法では、患者の血流からT細胞と呼ばれる免疫細胞を採取し、CARを用いて実験室で再プログラム化し、がん細胞表面のPSCAタンパク質を認識して攻撃するようにします。その後、CAR-T細胞を患者に再注入し、がん細胞を死滅させます。
前立腺がんは「免疫砂漠」と呼ばれています。腫瘍内部に侵入するT細胞が少ないため、腫瘍の星雲は免疫療法では治療が困難です。これを克服するには、非常に強力な何かが必要です。私たちの研究は、シティ・オブ・ホープの前立腺がんに対するCAR-T細胞療法が、この目標達成への一歩となる可能性を示しています。
Tanya Dorff 医学博士は、City of Hope の泌尿生殖器疾患プログラムの部門長であり、医学腫瘍学および治療研究部門の教授です。
「本研究の重要な知見は、PSCAを標的としたCAR-T細胞がmCRPCに対して安全かつ効果的であるということです」とプライスマン氏は付け加えた。「これは、現在他に有効な治療法がない患者のために、この種の細胞免疫療法のさらなる開発の可能性を開くものです。」
この試験の目的は、治療の安全性と用量制限毒性を調査し、患者に対する治療の有効性に関する予備データを取得することでした。
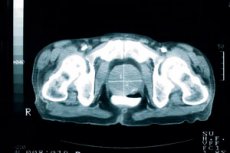
研究の結果:患者は、CAR T細胞治療の有効性を高めるために血液疾患の治療に日常的に使用されるリンパ球減少化学療法を受けることなく、1億個のCAR T細胞を1回注入された。これはCAR T細胞の初の臨床試験であったため、患者におけるCAR T細胞単独の安全性を評価することが重要であった。同量のCAR T細胞とリンパ球減少では、用量制限毒性の合併症である膀胱炎、または膀胱刺激が発生した。ドルフ氏は、PSCAは膀胱にも存在するため、CAR T細胞が膀胱細胞を攻撃して炎症を引き起こした可能性が高いと説明した。その後、研究者らは、この毒性を軽減するために、リンパ球減少を減らした新しいグループを研究に追加した。14人の患者のうち4人は、前立腺がん患者の病気進行の連続マーカーであるPSA値が低下し、そのうち1人は有意に低下した。画像は、治療を受けた患者のサブセットにおける治療反応を示した。 14人中5人に軽度から中等度のサイトカイン放出症候群が見られました。これは免疫細胞から血液中にサイトカインが大量に急激に放出されることで引き起こされることがあり、CAR T細胞を用いた治療後の一般的な副作用です。CRSは治療可能な副作用です。CAR T細胞は28日間の観察期間を超えて高レベルに持続しなかったため、治療の有効性が制限されていました。これは固形腫瘍の治療におけるCAR T細胞の分野では一般的な問題であり、研究者らは現在登録可能な治療法を用いてシティ・オブ・ホープで追跡研究を行い、この問題に取り組む予定です。以前にも数回治療を受けていたある患者は、CAR T細胞療法に良好な反応を示しました。彼のPSA値は95%低下し、骨と軟部組織のがんも縮小しました。彼は約8か月間、このような良好な反応を経験しました。
「患者さんの結果は非常に有望で、研究に参加してくださった患者さん、そして他の患者さんとそのご家族に深く感謝しています」とドルフ氏は述べた。「この治療を継続し、CAR-T細胞の数を増やしていくとともに、健康上の問題がないか注意深く観察し続けたいと考えています。そうすることで治療効果が向上すると考えています。」
抗腫瘍活性を高めるために放射線療法と組み合わせたPSCA CAR T細胞療法を使用するフェーズ1b臨床試験では、最大24人の患者を登録することを目指しています。
CAR-T細胞療法のリーダーとして認められているシティ・オブ・ホープは、1990年代後半にCAR-T細胞療法プログラムを開始して以来、約1,500人の患者を治療してきました。同施設は、世界有数のCAR-T細胞療法臨床試験プログラムを有しており、現在、13種類の固形腫瘍を含む約70件のCAR-T細胞臨床試験が進行中です。これらの臨床試験では、シティ・オブ・ホープが開発した治療法と企業の製品が使用されています。ネイチャー・メディシン誌に掲載された最近の研究では、シティ・オブ・ホープの脳腫瘍に対するCAR-T細胞療法が紹介されました。

