新しい出版物
LMU の研究者らは、ウイルスから体を守る上で重要な役割を果たす自然免疫受容体 Toll 様受容体 7 (TLR7) の周囲のさまざまな酵素の複雑な相互作用を解明しました。
免疫系の樹状細胞に存在するToll様受容体7(TLR7)は、ウイルスに対する自然防御において重要な役割を果たしています。TLR7は一本鎖ウイルスRNAやその他の外来RNAを認識し、炎症性メディエーターの放出を活性化します。この受容体の機能不全は自己免疫疾患においても重要な役割を果たすため、TLR7活性化のメカニズムを理解し、理想的にはそのメカニズムを調節することがますます重要になっています。
ミュンヘン遺伝学センターとLMU生化学科のファイト・ホルヌング教授とマレーネ・ベルーティ教授率いる研究者たちは、複雑な活性化メカニズムをさらに深く掘り下げることができました。これまでの研究から、受容体が認識するには複雑なRNA分子を切断する必要があることが分かっていました。
LMUの研究者たちは、細胞生物学からクライオ電子顕微鏡法に至るまでの幅広い技術を駆使し、一本鎖の外来RNAがどのように処理されてTLR7を検出するのかを解明しました。この研究はImmunity誌に掲載されました。
外来RNAの認識には多数の酵素が関与している
進化の過程で、免疫システムは病原体をその遺伝物質によって認識することに特化してきました。例えば、自然免疫受容体TLR7はウイルスRNAによって刺激されます。ウイルスRNAは、TLR7のリガンドとして認識するには大きすぎる長い分子鎖と考えることができます。ここでヌクレアーゼが登場します。ヌクレアーゼは「RNA鎖」を小さな断片に切断する分子切断ツールです。
エンドヌクレアーゼはRNA分子をハサミのように真ん中で切断し、エキソヌクレアーゼは鎖を一方の端からもう一方の端まで切断します。このプロセスにより、異なるRNA断片が生成され、TLR7受容体の2つの異なるポケットに結合できるようになります。受容体の両方の結合ポケットがこれらのRNA断片で満たされた場合にのみ、シグナル伝達カスケードが作動し、細胞を活性化して警戒状態を引き起こします。
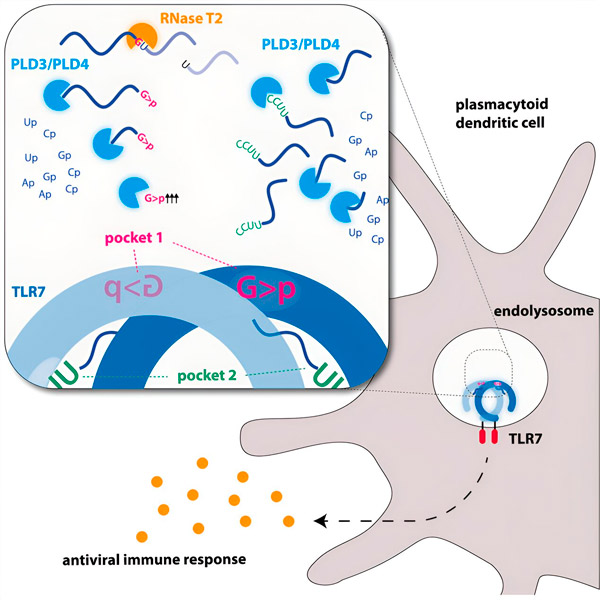
グラフィックイメージ。出典:Immunity (2024). DOI: 10.1016/j.immuni.2024.04.010
研究者たちは、TLR7によるRNAの認識には、エンドヌクレアーゼであるRNase T2の活性が必要であり、この活性はエキソヌクレアーゼであるPLD3およびPLD4(ホスホリパーゼD3およびD4)と連携して働くことを発見しました。「これらの酵素がRNAを分解できることは知られていましたが、今回、それらがTLR7と相互作用し、それによってTLR7を活性化することを実証しました」とホーヌング氏は述べています。
免疫システムのバランスを整える
研究者らはまた、PLDエキソヌクレアーゼが免疫細胞において二重の役割を果たすことを発見した。TLR7の場合は炎症促進作用を持ち、別のTLR受容体であるTLR9の場合は抗炎症作用を持つ。「PLDエキソヌクレアーゼのこの二重の機能は、適切な免疫反応を制御するための緻密に調整されたバランスを示唆しています」とベロウティ氏は説明する。
これらの酵素による炎症の同時刺激と抑制は、システムの機能不全を防ぐ重要な保護メカニズムとして機能する可能性があります。このシグナル伝達経路において他の酵素がどのような役割を果たすのか、そして関与する分子が治療の標的構造として適切であるかどうかは、今後の研究の課題となります。

