がんと診断された時点で、細胞レベルと分子レベルでは、気づかれずにすでに多くの出来事が起こっています。がんは臨床上、初期段階と後期段階に分類されますが、「初期」段階の腫瘍であっても、体内で以前に起こった、検出できない多くの変化の結果です。
現在、イェール大学医学部 (YSM) の科学者とその同僚は、強力な高解像度顕微鏡を使用して、マウスの皮膚細胞でがんを引き起こす最初の物理的変化を追跡し、これらの初期変化のいくつかを詳細に理解しました。
毛包でのがんの発達を促進する変異を持つマウスを研究することにより、科学者は、がん形成の最初の兆候が、マウスの毛包の成長の特定の時期と場所で発生することを発見しました。さらに、研究者らは、これらの前癌性変化は MEK 阻害剤と呼ばれる薬剤で阻止できることを発見しました。
研究チームは、YSM 遺伝学部の博士研究員である Tianchi Xin 博士が率い、YSM 遺伝学教授でイェール大学がんセンターおよびイェール大学幹細胞センターのメンバーである Valentina Greco 博士、およびジョンズ ホプキンス大学医学部の分子生物学および遺伝学の助教授である Sergi Regot 博士が参加しました。
研究結果は、Nature Cell Biology 誌に掲載されました。
科学者らは、ヒトで 2 番目に多い皮膚がんである皮膚扁平上皮がんを発症したマウスを研究しました。これらのマウスは、ヒトの癌で最も一般的に変異する癌遺伝子の 1 つである KRAS 遺伝子に癌を促進する変異を持つように遺伝子操作されました。KRAS 変異は、肺癌、膵臓癌、大腸癌でも発見されています。
科学者が研究した初期の変化には、前癌異常として分類される毛包の小さな異常な隆起が含まれています。「これらの初期イベントを理解することは、癌が最終的に形成されるのを防ぐためのアプローチを開発するのに役立ちます」と、この研究の筆頭著者である Xin 氏は述べています。
彼らの研究は皮膚癌に焦点を当てていますが、研究者は、関連する主要な遺伝子とタンパク質がさまざまな腫瘍で同じであるため、発見した原理は KRAS 変異によって引き起こされる他の多くの癌に適用できると考えています。
単なる細胞増殖以上のもの 人間とマウスの両方で、毛包は常に成長し、古い髪を脱ぎ捨てて新しい髪を形成します。幹細胞は、さまざまな種類の細胞に成長する能力があり、この再生プロセスで大きな役割を果たします。これまでの研究では、KRAS 変異が毛包における幹細胞の増殖の増加につながることが示されており、この幹細胞数の大幅な増加が前癌組織病変の原因であると考えられていました。
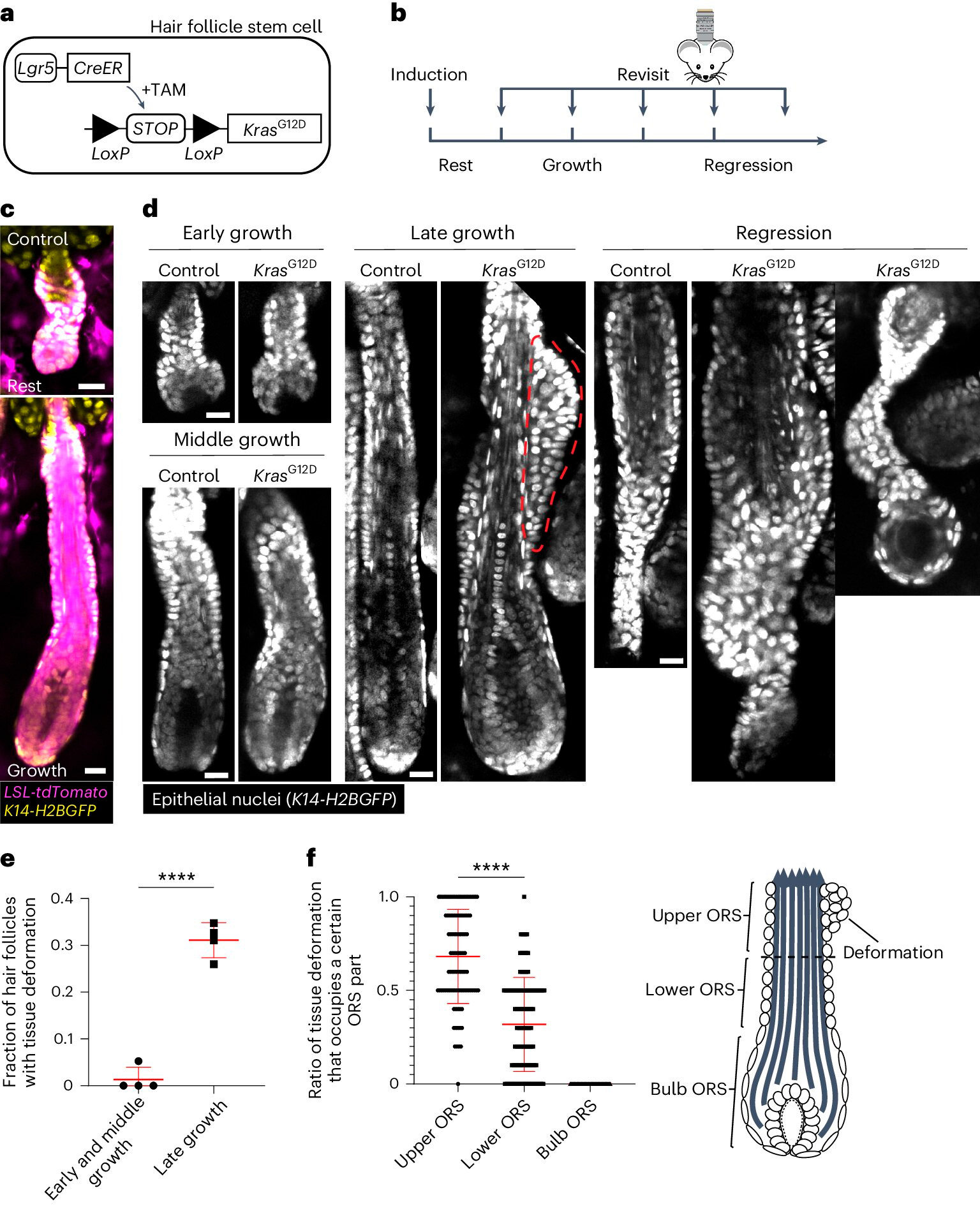
KrasG12D は、毛包再生中に時空間的に特定の組織変形を引き起こします。
a. タモキシフェン誘導性 Cre-LoxP (TAM) システムを使用して毛包幹細胞に KrasG12D を誘導する遺伝学的アプローチの概略図。
b. 毛髪成長サイクルの段階に関連して KrasG12D 誘導と再イメージングのタイミングを示す図。
c. Cre tdTomato (マゼンタ) 誘導性レポーターを含む、誘導後の野生型の休止期および成長期の毛包の代表画像。
d. 毛髪成長サイクルのさまざまな段階におけるコントロールおよび KrasG12D 毛包の代表画像。外毛根鞘 (ORS) の結節の形での組織変形は、赤い点線で示されています。
e. 毛包成長のさまざまな段階で組織変形を起こしている KrasG12D 毛包の割合。
f. 個々の KrasG12D 毛包の ORS の上部、下部、球状部を占める組織変形の割合。
出典: Nature Cell Biology (2024)。DOI: 10.1038/s41556-024-01413-y
この仮説を検証するために、研究チームは、動物の毛包の皮膚細胞で特定の時間に活性化できる、特別に設計された変異 KRAS を使用しました。 Xin 氏と彼の同僚は、生体内イメージングと呼ばれる顕微鏡技術を使用しました。この技術により、生体内の細胞の高解像度画像が撮影でき、動物の個々の幹細胞にタグを付けて追跡できます。
KRAS 変異が活性化されると、すべての幹細胞の増殖が速くなりましたが、前がん性の隆起は毛包の特定の 1 つの場所と成長の 1 つの段階でのみ形成されました。つまり、細胞数の増加がすべてではない可能性が高いということです。
毛包での KRAS 変異の活性化により、がんを促進する変異のない細胞と比較して、幹細胞の増殖が速くなり、移動パターンが変化し、さまざまな方向に分裂しました。
この変異は、ERK と呼ばれるタンパク質に影響します。Xin 氏は、生きた動物の個々の幹細胞で ERK の活動をリアルタイムで観察し、KRAS 変異によって引き起こされるこのタンパク質の活動の特定の変化を発見しました。研究者らは、ERK の活性を阻害する MEK 阻害剤を使用して、前癌性の隆起の形成を止めることもできました。
この薬剤は、細胞の移動と配向に対する変異の影響を止めましたが、幹細胞の増殖全体に対する影響は止めませんでした。つまり、前癌状態の形成は、これらの最初の 2 つの変化によるものであり、細胞増殖の増加によるものではないということです。
文脈における前癌性変化 研究者らがこれらの原理を発見できた唯一の方法は、生体内での発癌性変異の影響をリアルタイムで追跡することです。これは重要です。なぜなら、癌は真空中で形成されるのではなく、成長して維持するために微小環境に大きく依存しているからです。科学者らは、個々の細胞の行動だけでなく、それらの細胞内の分子も追跡する必要がありました。
「これらの発癌性イベントを理解するために私たちが採用したアプローチは、実際にはスケールを超えてつながることです」と Greco 氏は言います。 「シン博士がレゴット博士と共同で使用したフレームワークとアプローチにより、分子要素まで掘り下げて、それらを細胞と組織のスケールに結び付けることができました。これにより、生体外では達成するのが非常に難しいこれらのイベントの解決が可能になります。」
研究者たちは現在、最初の隆起が形成された後に何が起こるかを確認するために、より長い期間にわたってプロセスを追跡したいと考えています。彼らはまた、炎症などの他の発癌性イベントを研究し、発見した原理が他の状況にも当てはまるかどうかを確認したいと考えています。

