フランクフルトのゲーテ大学が実施した研究は、サリドマイド誘導体が癌治療に使用できる可能性を示唆しています。サリドマイドは1950年代に睡眠薬として販売されていましたが、後に妊娠初期に重度の先天異常を引き起こすことで悪名高い存在となりました。
この分子は細胞内のタンパク質を破壊対象として標識することも知られています。本研究の一環として、科学者たちはサリドマイドの誘導体を作製しました。そして、これらの物質が癌細胞の生存を担うタンパク質の破壊に作用することを実証しました。
サリドマイドほど波乱に満ちた歴史を持つ分子は他にないでしょう。1950年代に多くの国で鎮静剤および睡眠薬として承認された薬の主成分でした。しかし、サリドマイドを服用した妊婦から、重度の奇形児が出産するケースが多いことがすぐに明らかになりました。
しかし、ここ数十年、医学界は再びこの薬に大きな期待を寄せています。研究によって、特に血管の成長を阻害し、腫瘍を栄養培地から切り離すのに適している可能性が示されました。さらに、骨髄の悪性腫瘍である多発性骨髄腫の治療にも非常に効果的であることが証明されました。
「サリドマイドは『分子接着剤』と呼べることがわかりました」と、フランクフルト・ゲーテ大学薬化学研究所の鄭星来博士は説明する。「つまり、サリドマイドは2つのタンパク質を掴んで結合させることができるのです。」
これが特に興味深いのは、これらのタンパク質の 1 つが一種の「ラベリング マシン」であり、別のタンパク質に明確な「GARBAGE」ラベルを付けるからです。
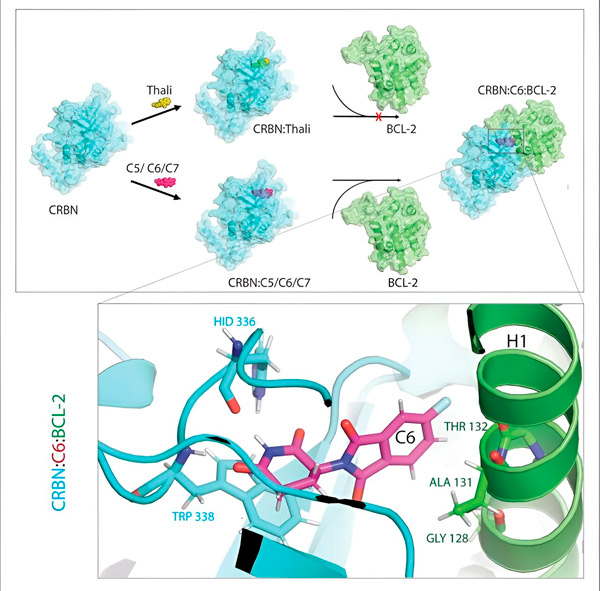
サリドマイド誘導体C5、C6、C7は、「標識装置」であるCRBNを改変し、BCL-2に結合できるようにします。これにより、BCL-2分子は分解されるように標識されます。これは、がんと闘うための新たな戦略となる可能性があります。著者:Xinglai Cheng博士
細胞の廃棄物処理システムはこのタグを認識し、タグが付けられたタンパク質分子を捕らえて細断します。「このメカニズムがサリドマイドの様々な作用を説明しています」とチェン氏は言います。「どのタンパク質がタグ化されるかによって、胚発生中に奇形を引き起こしたり、悪性細胞を破壊したりします。」
このメカニズムは、がん細胞が生存するために特定のタンパク質に依存していることから、医療に大きな可能性をもたらします。もしこれらのタンパク質を体系的に標的とし、破壊することができれば、がんを治癒できる可能性があります。問題は、この分子接着剤が非常に特殊であることです。
結合パートナーの1つは常に細胞の標識装置、つまり科学用語でCRBNと呼ばれるE3リガーゼです。体内に存在する数千種類のタンパク質のうち、2つ目のパートナーになれるのはごくわずかで、どれが2つ目のパートナーになるかは接着剤の種類によって異なります。
「そこで、私たちは一連のサリドマイド誘導体を作製しました」とチェン氏は語る。「そして、それらが接着性を持つかどうか、そしてもし持つならどのタンパク質に対して有効かを試験しました。」研究者たちは、培養細胞株中のすべてのタンパク質にこれらの誘導体を添加しました。そして、CRBNの存在下でこれらのタンパク質のうちどれが分解されるかを観察しました。
「この過程で、分解に非常に重要な細胞タンパク質であるBCL-2にタグを付けることができる3つの誘導体を特定しました」とチェン氏は説明する。「BCL-2は細胞が自己破壊プログラムを活性化するのを阻害するため、BCL-2がなければ細胞は死滅します。」
そのため、BCL-2は長らく癌研究の焦点となってきました。BCL-2の効力を低下させ、変異細胞の自滅を促す白血病治療薬「ベネトクラックス」さえ存在します。
「しかし、多くのがん細胞ではBCL-2自体が変異しています。その結果、ベネトクラックスはもはやこのタンパク質を阻害しなくなります」とチェン氏は語る。「私たちは、この誘導体もこの変異体を分解対象として標識することを示すことができました。さらに、マックス・プランク生物物理学研究所のパートナーは、サリドマイド誘導体とBCL-2の相互作用をコンピューター上でシミュレーションしました。その結果、誘導体はベネトクラックスとは全く異なる部位に結合することが示され、後に実験的に確認することができました。」
研究者らは、がん細胞を持つショウジョウバエにも化合物を投与した。この方法で治療されたショウジョウバエの生存率は有意に向上した。しかし、チェン氏は、これらの結果はまだ基礎研究段階であるため、過度の期待は禁物だと警告する。「これらの結果は、改変されたサリドマイド分子が大きな治療効果を持つことを示していますが、将来的に実際にその効果が実証されるかどうかはまだ分かりません。」
この研究の結果は、Cell Reports Physical Science 誌に掲載されました。

