新しい出版物
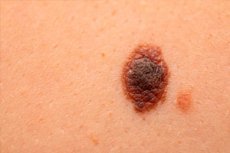
Nutrients誌は、食事がメラノーマのリスク、経過、そして治療反応に及ぼす影響に関する数十件の研究をまとめた包括的なレビューを発表しました。著者らは、脂質(特にオメガ3およびオメガ6多価不飽和脂肪酸)、ビタミン、抗酸化物質、植物性生理活性化合物、そして別枠で、腫瘍の悪性度と免疫療法の有効性の両方に関連する腸内細菌叢の役割を検証しています。その要点は、紫外線が依然として第一の要因であるものの、食生活は酸化ストレス、炎症、そして免疫反応を変化させる能力があり、したがって理論的にはメラノーマの転帰に影響を与えるというものです。厳密な推奨を行うには十分なエビデンスはまだありませんが、既に方向性は示されています。
研究の背景
黒色腫は依然として最も悪性度の高い皮膚腫瘍の一つです。主なリスク要因は紫外線(特に小児期および青年期における反復性熱傷)と考えられており、遺伝的脆弱性(色白の肌/髪、多発性母斑、家族歴、MAPK経路(BRAF/NRAS)の変異)を背景にしています。しかし、紫外線に加えて、慢性炎症、代謝変化、免疫監視といった全身的環境因子の役割についても、長年にわたり議論されてきました。これらの因子は、日常の栄養摂取によって大きく影響を受けます。これにより、議論は光の「局所的」影響から、腫瘍が増殖しやすい、あるいは逆に腫瘍が定着しにくい体質へと移行しています。
栄養生物学の観点から見ると、2つの主要な回路が重要です。1つ目は酸化ストレスと炎症です。過剰な飽和脂肪酸とオメガ6系多価不飽和脂肪酸(「西洋」食生活に典型的)は、免疫抑制と腫瘍増殖に関連するPGE₂などのエイコサノイドの産生を促進します。一方、オメガ3系(EPA/DHA)と植物性ポリフェノールは、抗炎症メディエーターとしてのバランスを変化させ、抗酸化防御を強化します。2つ目は腸内細菌叢です。適切な食物繊維の摂取は、短鎖脂肪酸(主に酪酸)の産生を促進します。短鎖脂肪酸はバリアを強化し、T細胞応答を制御します。また、悪性黒色腫患者の臨床研究によると、チェックポイント阻害剤による免疫療法への反応改善にも関連しています。
観察研究はますます一貫した見解を示しつつあります。植物由来の抗炎症性食生活(野菜、果物、全粒穀物、ナッツ/種子、魚、オリーブオイル)は、より良好な免疫炎症プロファイルと「健康な」マイクロバイオームと関連しています。一方、過剰な糖分、オメガ6脂肪酸、食品添加物を含む超加工食品は、腸内細菌叢の乱れや慢性の低レベルの炎症と関連しています。しかし、カプセルに入った抗酸化サプリメントに関するエビデンスは依然として不明確であり、高用量摂取において中立的な影響と潜在的な有害作用の両方が報告されています。そのため、レビューの焦点は個々の錠剤からホールフードへと移行しています。
臨床的エビデンスは依然として断片的であり、因果推論は限られており、介入試験は小規模でデザインも不均一です。しかしながら、論理的な「軸」が浮かび上がりつつあります。それは、食事 → 微生物叢/代謝物 → 炎症と免疫監視 → メラノーマのリスク/行動と治療への反応です。この文脈において、本レビューはメカニズムと臨床のシグナルを体系化し、慎重ながらも実践的な方向性を策定しています。炎症を軽減し、微生物叢代謝物(SCFA)をサポートする食事は、理論的にはがんの転帰を改善する可能性がありますが、日焼け対策と標準的な治療は依然として優先されるべきです。
なぜこれが重要なのでしょうか?
メラノーマは最も悪性度の高い皮膚がんの一つであり、患者から「日焼け対策以外にどのような生活習慣の改善ができますか?」という質問がよく寄せられます。このレビューは、異なるエビデンスを巧みに結び付けています。オメガ3脂肪酸と抗酸化物質を豊富に含む植物由来の「抗炎症」食は、炎症と免疫反応のプロファイルを良好に保つことが示唆されています。一方、加工食品や飽和脂肪酸/オメガ6脂肪酸の過剰摂取は、炎症誘発性シグナル伝達の増加と関連しています。また、食物繊維と腸内細菌叢が、メラノーマ治療の鍵となる薬剤であるチェックポイント阻害剤への反応をどのようにサポートするかについても、関心が高まっています。
データが示すもの - セクション別
酸化ストレスと抗酸化物質。メラノサイトは、紫外線とメラニン生合成の「キッチン」自体から発生するROS(活性酸素種)の影響を受けやすい。抗酸化物質と植物ポリフェノールを豊富に含む食事は、理論的にはこの背景ストレスを軽減し、腫瘍の発生と進行を抑制する可能性があるが、臨床的なエビデンスは散在している。
炎症と脂肪。重要なのは「脂肪の量」ではなく、どのような種類の脂肪を摂取するかです。オメガ6脂肪酸(植物油、加工食品)は、免疫抑制と腫瘍の増殖に関連するアラキドン酸/プロゲステロン(PGE₂)経路を促進します。一方、オメガ3脂肪酸(EPA/DHA)はPGE₂を減少させ、T細胞応答を促進し、前臨床研究では腫瘍の増殖と転移を阻害することが示されています。オメガ6脂肪酸とオメガ3脂肪酸のバランスは、脂肪自体の割合よりも重要です。
植物性生理活性化合物。野菜、果物、ナッツ、オリーブオイルに含まれるポリフェノール、フラボノイド、カロテノイドはNF-κBを阻害し、炎症性サイトカインの産生を抑制し、内因性抗酸化防御を強化します。これは、観察研究において地中海式ダイエットが癌の予後改善と関連付けられているメカニズムの一つです。
腸内細菌叢と免疫療法。高繊維食は、主に酪酸を産生する短鎖脂肪酸(SCFA)を産生する細菌の働きを補助します。SCFAはT細胞免疫を調節し、臨床シリーズおよび小規模コホート研究において、メラノーマ患者におけるPD-1/PD-L1阻害剤への反応改善との関連が示されています。これは自己治療のガイドではなく、臨床試験の指針です。
これは「今日の写真」にどう当てはまるだろうか
要約すると、本レビューからは明確な「軸」が浮かび上がります。それは、食事 → 微生物叢/代謝物 → 炎症/免疫 → 腫瘍の挙動と治療への反応です。ほとんどの研究で示されている防御ベクトルは、植物性食品(野菜、果物、全粒穀物、ナッツ/種子、魚)中心のパターンと、適度な動物性脂肪および加工肉の摂取です。対照的に、オメガ6脂肪酸、糖類、加工食品を過剰に摂取する西洋型の食事は、免疫監視にとって不利な炎症誘発性の変化と関連しています。同時に、著者らは因果関係が証明されておらず、大規模な前向き研究とRCTが必要であることを強調しています。
候補者リスト - 何が有望で何がリスクがあるか
有望な栄養ハイライト(医学的アドバイスではありません):
- 週に2〜3回、脂肪分の多い魚(EPA/DHAの供給源)
- 野菜・果物、全粒穀物、ナッツ・種子を毎日摂取する(ポリフェノール+食物繊維→SCFA)
- 基礎脂肪としてのオリーブオイル
- 繊維を 25 ~ 35 g / 日 (許容できる範囲) まで「伸ばす」。
制限するもの:
- 過剰な加工肉と精製糖
- オメガ6過剰摂取の油/加工食品(エイコサノイドのバランスを変化させます)
- 「長い」成分を含む超加工食品。
「ダイエット+セラピー」が特に興味深いのは
- 免疫療法期間: チェックポイント阻害剤に対する繊維/SCFA と微生物叢の多様性の役割に関するデータは、研究環境における注意深い食事介入を推奨します (治療の代わりではありません)。
- リスクグループにおける予防: 母斑が複数ある人、家族歴がある人、紫外線に多くさらされている人は、炎症や酸化ストレスに対する「基本設定」として地中海パターンを検討するとよいでしょう。
限界と今後の展望
著者らは率直にこう述べている。「データが不足しており、結果は多岐にわたり、臨床試験は小規模で異質であるため、すべてのメラノーマ患者に対する食事指導を策定することはまだ不可能です。バイオマーカー(炎症、短鎖脂肪酸、微生物叢)と「明確な」エンドポイント(リスク、生存、ICTへの反応)を用いた大規模な前向き研究プロジェクトと介入研究が必要です。しかしながら、保守的ながらも実践的な推奨事項は既に現れつつあります。それは、炎症を「鎮静」し、微生物叢に栄養を与える栄養は、腫瘍学的目標と論理的に組み合わせられるというものです。」
出典:アビゲイル・E・ワトソン、ナビハ・ユスフ「メラノーマの発生と進行に対する食事因子の影響:包括的レビュー」 Nutrients 17(11):1891. https://doi.org/10.3390/nu17111891

