新しい出版物
08 August 2025, 17:49
関節リウマチ(RA)患者の中には、生物学的製剤や標的合成DMARD(DMARD)が十分な効果を発揮しない、あるいは忍容性が低い患者がいます。こうした背景から、迷走神経を介した神経免疫調節のためのインプラントであるSetPointシステムが米国で承認されました。
承認されるものは何ですか?
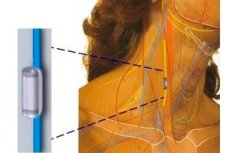
SetPointシステムは、迷走神経に1日1回短時間の電気刺激を与え、生来の抗炎症および免疫回復経路を活性化する埋め込み型デバイスです。適応症:中等度から重度の関節リウマチ(RA)患者で、先進治療(バイオ医薬品/多剤耐性DMARD)による治療が不十分、または忍容性が低い患者。
エビデンスベース(RESET-RA)
ランダム化RESET-RA研究では、242人の患者が実際のインプラントまたは「ダミー」デバイスのいずれかを装着しました。
- 主な目標は達成されました: 3 か月目までに ACR20。
- さらに、最大 12 か月の追跡調査で活動指標と応答率が向上しました。
- 参加者の 75% は 12 か月までに生物学的製剤/標的合成 DMARD の服用を中止しました。
- 処置と治療は忍容性に優れており、重篤な有害事象は 1.7% でした。
安全性と利便性
設置は低侵襲の外来手術です。デバイスは埋め込まれるとプログラムされ、スケジュールに従って自動的に刺激を送ります。また、最長10年間使用できるように設計されています。
これは実践にとって何を意味するのでしょうか?
- RA 治療の新しいクラス、DMARD の代替/追加としての神経免疫調節が登場しました。
- 高度な治療法に対する反応が不十分な患者や耐性のない患者では、検討するのが妥当です。
- 実際の臨床実践データと、長期的な有効性/安全性に関する有効薬剤との比較、および反応患者の選択基準が必要です。
著者のコメント
「SetPointの承認は、神経経路を利用して炎症と闘うという、自己免疫疾患への新たなアプローチとしての神経免疫調節の可能性を浮き彫りにするものです」と、RESET-RA(ハーバード大学)の主任研究者であるマーク・リチャードソン医学博士は述べています。
「このデバイスは一度埋め込まれると、最大10年間、設定されたスケジュールに従って自動的に治療を行うので、RA患者の生活が楽になります」と彼は付け加えた。

