記事の医療専門家
新しい出版物
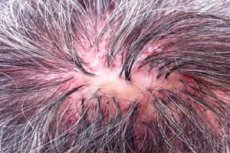
頭皮萎縮性毛包炎(別名:頭部萎縮性毛包炎(folliculitis sycosiformis atrophicans capitis、Hoffmann E. 1931)は、Quinquaud(Quinquaud Ch.E. 1889)によって初めて記載されました。この非常にまれな皮膚病は、頭皮の慢性細菌性毛包炎であり、萎縮性脱毛症(偽毛包状態、decalvo(ラテン語)-禿げる)に終わります。皮膚の他の部分も影響を受ける可能性があり、特に剛毛で長い髪で覆われている部分です。顔のひげの成長領域で同じ年に記載された同様のプロセスには、別の名前が付けられました:ルポイド白癬(sycosis lupoides、Brocq L.、1888)、瘢痕性白癬状紅斑(ulerythema sycosiforme、Unna P.、 1889年。 ovkr (ギリシャ語) = ule (ラテン語) = 傷跡);毛嚢状萎縮性毛嚢炎(毛嚢炎 sycosiforme atrophicans barbae、Hoffmann E.、1931)。
そのため、異なる科学者が同じ皮膚病に異なる名前を付けましたが、その中で、それぞれの視点からの主な特徴が強調されていました。慢性毛包炎は、経過と結果が円板状エリテマトーデス(萎縮)に似ています。シコシ状の症状と瘢痕を伴う紅斑。慢性毛包炎は、シコシスに似ていますが、萎縮につながります。デカルバン毛包炎とルポイドシコシスの最初の説明ですでに、両方の皮膚病に共通の特徴が明らかにされ、臨床症状が決定されました。慢性毛包炎は、膿疱や潰瘍を伴わずに萎縮と持続性脱毛症につながり、治療に非常に抵抗性です。違いは、慢性毛包炎の分布(形成された大きな個々の病巣と比較して、小さな病巣にまとめられた毛包炎)と主な場所(頭皮または顔の皮膚)にあります。その後、顔面皮膚に加えて、ルポイド白癬(LS)は頭皮、陰部、腋窩部の皮膚にも影響を及ぼすことが判明しました。そして、数年後になってようやく、Brokが報告したルポイド白癬は独立した病理学的病型ではなく、同じ疾患の重複であることが明らかにされました。デカルバン毛包炎は、独特でまれな臨床的変異です。
毛包炎の原因
原因菌は黄色ブドウ球菌と考えられており、毛包へのグラム陰性細菌の定着も考えられます。しかし、広域スペクトル抗生物質による治療は一時的な治療効果しか得られず、その効果は投与期間によって厳密に制限されます。これは、マクロファージの優位性、その反応性の変化、そして免疫防御力の低下を裏付けています。
病因
脂漏性疾患、糖尿病による抵抗力の低下、慢性腎炎、異常タンパク血症、その他免疫抑制につながる要因が、この皮膚疾患の発症要因となる可能性があります。歯周炎を合併した齲蝕歯の除去後にデカルバン毛包炎(DF)が自然治癒した症例が報告されています。毛包への細菌の定着は、おそらく病因的な要因に過ぎません。慢性毛包炎が皮膚萎縮と持続性脱毛症に至る理由は依然として不明です。デカルバン毛包炎、またはルポイド白癬の患者においては、現代の研究手法により、免疫系、内臓、その他の身体系の機能における特異的かつ重大な障害が常に検出されています。
ケンコ毛包炎の症状 デカルバン
デカルバン毛包炎は通常、頭皮、主に側頭および頭頂部に孤立して発生し、前頭部の病変は発毛の境界に位置し、蛇行に似ています。場合によっては、腋窩および恥骨領域も影響を受けます。炎症性毛包結節の発疹(膿疱は少ない)は、通常、主観的な感覚を引き起こさないため、目に見えることがよくあります。発疹要素のサイズは、ピンの頭からレンズ豆までさまざまです。中央では、丘疹および膿疱要素に変化のないまたは折れた髪が浸透し、その周囲に小さな充血の冠が見られます。毛包炎は非常にゆっくりとした発達を特徴としており、目立ったダイナミクスなしに長期間存在し、膿疱の形成で終わらないことがよくあります。個々の毛包性膿疱は、毛包性丘疹(Mashkilleyson LN, 1931によれば「二次性膿疱」)の長い進化の後にのみ出現する。小さな集団の病巣の中心には、持続性脱毛を伴う軽度の瘢痕性萎縮が徐々に形成される。隣接する複数の病巣が融合すると、より大きな瘢痕性脱毛症の病巣が形成され、その中に個々の毛髪が保存されることもある。境界領域では、新たな毛包結節や膿疱、鱗屑、痂皮が出現し続け、周辺の成長が緩やかになる。このように、デカルバン毛包炎は、様々な大きさや形状の萎縮性脱毛症の病巣(偽脱毛症)の形成につながる。皮膚疾患の経過は慢性的で、数年から数十年にわたり持続する。萎縮性脱毛症の病巣の周囲に出現する新たな毛包炎の数は、最小限に抑えられる場合もある。頭皮のデカルバン毛包炎は、顔面皮膚またはその他の部位の狼瘡性白癬 (LS) の病巣と併発することがあります。
狼瘡性白癬は、主に中高年の男性に発症します。狼瘡の1つまたは2つの病巣は通常、毛深い頬、こめかみの側面にあり、まれに顎や上唇にも発生します(Milman IS、1929)。病変はほとんどの場合片側性で、側頭葉の毛が生える領域、または下顎の水平枝と上行枝の上の頬に位置します。狼瘡の病変は、大きな単一の病変として単独で発生することもあれば、頭皮に発生することもあります。最初は、充血を背景に、同じ領域に集まった炎症性の毛包結節と膿疱、および毛包に位置する小さな淡黄色の痂皮と灰色がかった鱗屑が現れ、これらはこすり取ることで簡単に除去できます。これらの要素が融合して、直径2〜3 cm以上の明確な円形または楕円形の炎症性プラークを形成し、色はワインレッド色(類丹毒の場合のように)で、基部に平坦で痛みのない浸潤があります。徐々に、その中心部の皮膚は青白く、薄くなり、滑らかになり、毛がなく、わずかに陥没します。形成された狼瘡性白癬の特徴的な特徴である中心萎縮が発症します。その範囲内では、新しい発疹は現れなくなり、1つまたは複数の毛包から成長する単一の毛または毛束がまだ残っている場合があります。幅約1 cmの病巣の周辺領域はわずかに隆起し、赤色がより飽和し、中程度に浸潤しています。まれに毛包性膿疱を伴う多数の毛包性丘疹があり、そのいくつかは泡として知覚されます。これらの要素の中心部には、まだ残っている毛髪(一部は折れている)に加え、容易に除去できる毛包に位置する痂皮や鱗屑が多数存在します。病変は、周辺部に新たな毛包炎と個々の毛包性膿疱が出現することにより、徐々に大きくなります。病変の成長が病巣の一つに集中し、円形の輪郭が変化する場合もあります。病変の縁を鏡検しても、「リンゴゼリー」症状は確認できません。LSは数ヶ月から数年にわたって慢性的に進行します。頭皮のルポイド白癬の臨床症状はより滑らかです。形成された病変では、滑らかで毛のない萎縮領域が優勢です。周辺部では隆起した隆起は見られず、充血の狭い縁に囲まれた個々の長期にわたる毛包炎と膿疱、そして孤立した小さな鱗屑や痂皮のみが見られます。したがって、頭皮においては、ルポイド性白癬とデカルバン毛包炎の症状は実質的に区別がつきません。患者の全身状態は悪化しておらず、主観的な感覚は通常見られず、訴えは美容上の欠陥に限られます。
組織病理学
表皮には、小さな局所的な角質増殖、角質の擦り切れた塊、顕著な表皮肥厚が認められる。有棘層の細胞は、特に下層において顕著に変化し、顕著な空胞性ジストロフィーの兆候が見られる。毛包の開口部は著しく拡張し、角質塊で満たされている。真皮には、血管周囲および毛包周囲のリンパ組織球浸潤が密集しており、稀に形質肥満細胞および好中球が認められる。場合によっては、浸潤はほぼ完全に形質細胞で構成される。最終的な萎縮期においては、病理形態学的所見は、後期の偽毛包病変の特徴的な変化とほとんど変わらない。
ケンコのデカルバン毛包炎の診断
頭皮におけるデカルバン毛包炎またはルポイド白癬の症状は、主に慢性毛包炎および毛包性膿疱として現れ、偽毛包状態に至る疾患と区別されます。したがって、病変の中心部に毛包真菌症(DFまたはLS)の萎縮が形成されていない場合は、鱗屑状毛包炎、尋常性白癬、そして後に壊死性座瘡、毛包炎および毛包周囲炎(ホフマン頭を膿瘍化および陥入)、ランゲルハンス細胞の組織球症、びらん性膿疱性皮膚症を伴う)を含む頭皮真菌症と区別されます。頭皮の毛包性丘疹および結節は、慢性毛包炎および膿疱に類似することがあります。また、毛包性扁平苔癬、エリテマトーデス、ループス結核症、ルポイドリーシュマニア症、結核性梅毒とも鑑別されます。病変の活動性末梢部における典型的な発疹要素(毛包炎、膿疱など)の組織学的検査は、最終診断を確定する上で重要な助けとなります。
頭皮真菌症の鑑別診断。真菌学的検査の対象となるのは、頭皮に剥離、変質した毛髪、黄色のかさぶた状の鱗屑、毛包膿疱、炎症性の毛包結節および結節、毛髪の断片を伴う化膿性血性痂皮、そして様々な大きさの瘢痕性脱毛症の病巣がある場合です。これらの症状が認められる場合、特に小児および高齢者では、頭皮真菌症を除外することが推奨されます。皮膚の他の部位を検査する際は、手足の爪甲の状態にも注意してください。毛髪の蛍光検査、毛髪の変質、皮膚および爪の鱗屑、痂皮、膿性分泌物の顕微鏡検査および培養検査を実施する必要があります。最も迅速かつ有益な診断方法は、変質した毛髪(皮膚レベルで折れ、「黒い点」のように見え、高さ3~5mmで、根元にキャップがあり、灰色で鈍く、「斑点」や「感嘆符」の形に変形している)の顕微鏡検査です。真菌要素の検出と、それによって毛髪病変の特徴を明らかにすることで、医師は頭皮真菌症を診断し、病原体の属と疾患の疫学的な可能性を把握することができます。
ルポイド白癬(LSまたはDF)は、長期毛包炎が優勢である点で、下品な白癬とは異なります。その一部のみが毛包膿疱の形成で終わり、1つまたは2つ(DFの場合はそれ以上)の明確な病巣が存在し、周辺部の成長が遅いこと、およびその中に2つの領域(頭皮の病巣を除く)が存在します。中心の広い瘢痕性萎縮領域と、新しい毛包炎が形成される赤い隆起の形で蛇行する周辺領域です。LSの特徴的な局在も異なり、頬の側頭部と側面、頭皮、そしてそれほど頻繁ではありませんが、下品な白癬に好発する顎と上唇です。また、DS(またはDF)は尋常性白癬と比較して治療抵抗性が高いこと、そして病理形態学的所見の相違も考慮する必要があります。DF(またはDS)では、臨床診断および組織学的診断において重要な頭皮の活動性周辺領域が弱く発現しており、個々の毛包炎および毛包性膿疱のみで表されます。このように、デカルバン毛包炎、またはルポイド白癬は、他の多くの頭皮皮膚疾患とは異なり、偽毛包状態へと至ります。
頭皮のデカルバン毛包炎(またはルポイド白癬)は、壊死性座瘡(NA)またはこの部位の壊死性毛包炎と区別する必要があります。これらのまれな皮膚疾患は、共通の主要な発疹要素(毛包炎)と慢性の経過をたどりますが、毛包炎の局在と分布、および進化の速度と特徴が異なります。DFまたはLSの場合、壊死性座瘡とは対照的に、直径2〜5 mmの長期にわたる毛包性丘疹が特徴であり、中心壊死や汚い茶色の壊死性痂皮のない単一の膿疱にゆっくりと変化します。DFまたはLSでは、慢性毛包炎が集まって周辺的に成長し、膿疱化、中心壊死、掻痒を伴わずに融合し、萎縮性脱毛症(偽毛包状態)の滑らかな病巣の形成につながります。たとえば、NUでは、好ましい局在は、額の毛の成長境界に沿った皮膚(生え際の外側と内側の数センチの幅の領域)、側頭部、首の後ろですが、まれに発疹が耳、鼻、胸部と背中の中央部に広がることがあります。壊死性ざ瘡では、毛包炎は、通常、脂漏性状態を背景に高齢者に発生し、掻痒を伴い、すぐに丘疹膿疱性に、次に丘疹壊死性要素に変化します。それらは常に孤立しており、互いに境界が定まっており、末梢には成長せず、したがって大きな病巣に融合しません。NUでは、直径2〜4 mmの紫赤色の毛包性丘疹と丘疹膿疱が、中心部で急速に壊死し、汚れた茶色の壊死性痂皮で覆われます。これらはしっかりと付着し、長期間持続するため、臨床症状の大半を占め、壊死性ざ瘡または壊死性毛包炎の最も特徴的な症状です。かさぶたが剥がれた後、孤立したスタンプ状の天然痘のような瘢痕が皮膚に残り、丘疹壊死性結核または群発結核性梅毒後の瘢痕に似ています。頭皮では、NU後の瘢痕はほとんど目立たず、すぐに検出できる瘢痕性萎縮の病巣の形成にはつながりません。これらの皮膚疾患の組織学的変化も異なります。壊死性ざ瘡の組織学的像の特徴は、毛包内の毛包漏斗部上皮の壊死を伴う顆粒球膿瘍の位置です。毛包周囲の浸潤は、好中球、リンパ球、肥満細胞で構成され、末梢炎症領域に血管血栓があります。
頭皮の毛包炎および毛包周囲膿瘍およびホフマン剥離(FPAP)の初期症状は、デカルバン毛包炎(DF、またはルポイド白癬)に類似する場合があります。しかし、形成された臨床症状では、これらの皮膚疾患の類似性はほとんどなく、毛包の慢性炎症と瘢痕性脱毛症につながる長期にわたる持続的な経過に限られています。病変の深さ、毛包領域の炎症変化、主な発疹要素とその進行は異なります。DF(またはLS)では、頭皮の表在性慢性毛包炎がグループ化され、膿疱化、皮下膿瘍リンパ節の形成、および膿性血性分泌物と瘻孔の形成なしに、病巣に融合します。病変の中心部、最も広い領域に、滑らかで光沢のある薄い萎縮性瘢痕(偽鱗屑状状態)が形成されます。病変の辺縁部では、周囲に単一の膿疱と充血の縁、および容易に剥離できる鱗屑と痂皮を伴う毛包性丘疹が優勢です。 FPAP では、DF(または LS)とは対照的に、主な発疹要素は直径 0.5~1.5 cm の深部リンパ節であり、これが組織を融合、膿瘍化、穿孔します。これらは、深部膿瘍および皮膚の剥離を伴う毛包炎および毛包周囲炎の進行の結果として発生します。リンパ節が膿瘍化すると、多数の皮下瘻管が形成され、皮膚を剥離し、表面に多数の開口部が開いているように見えます。凹凸のある表面で浸潤部を押すと、互いに間隔を置いた複数の瘻孔から膿性および血性の分泌物が同時に排出されます。これは、このまれな皮膚疾患の特徴と考えられています。深く(腱ヘルメットまで)穿通した病変は、頭皮の顕著な充血を伴わず、わずかな痛みを残すことは注目に値します。FPAPは、顕著な脂漏性状態にある20~30歳の男性にのみ発生します。場合によっては、この皮膚疾患は球状および逆性のざ瘡を併発します。個々のFPAP病巣の瘢痕化後、萎縮性脱毛症だけでなく、特に後頭部に肥厚性の凹凸のある瘢痕が残ります。
頭皮のランゲルハンス細胞組織球症は、この部位の毛包炎、または狼瘡性白癬の症状と臨床的に非常に類似する場合があります。これらの疾患は慢性で、着実に進行し、偽毛包状態へと移行します。この状態では、以前の皮膚疾患の特徴的な症状は維持されません。一部の患者では、頭皮の組織球症による病変は孤立性ですが、多くの場合、皮膚や目に見える粘膜におけるランゲルハンス細胞の増殖、または他の組織(骨、中枢神経系、肝臓、眼窩内など)におけるマクロファージの増殖によって引き起こされる全身的変化の一部です。これらの症例では、皮膚組織球症の一般的な症状(ダリエ病、デカルバン毛包炎、壊死性座瘡など、他の皮膚疾患の症状と類似する場合もあります)に加えて、この非常にまれな疾患には他の特徴的な症状も見られます。最も一般的な症状は、肺病変、骨(特に頭蓋骨)の破壊巣、下垂体後葉の損傷(尿崩症の症状として現れる)、眼球後部への脂肪組織の浸潤による眼球突出、口腔粘膜の損傷(歯肉の浸潤と腫脹、潰瘍、歯の動揺と脱落)です。頭皮組織球症とダリエ病の臨床症状が非常に類似している症例もあります。
頭皮のこれらの皮膚疾患の臨床症状は非常に類似しているため、DFの特徴ではない個々の症状を区別することが可能です。最も重要な違いは、頭皮の皮膚組織球症の活動領域に毛包に関連しない丘疹膿疱性および膿疱性要素が存在すること、および痂皮が剥がれた後に現れる細長い形状の個々の表層びらんおよび潰瘍です。これらのわずかに痛みを伴う表層欠損は、細長い形状(幅最大0.5 cm、長さ最大1 cm)で、表面が不均一で、皮膚レベルよりわずかに突出しています。これらの要素の進化は、さまざまなサイズと形状の皮膚萎縮領域の発生につながり、脱毛の萎縮性病変の周囲に位置し、時にはレースの形をしており、この領域の髪の毛が著しく薄くなります。おそらく、組織学的確認なしに診断されたDF患者の一部に見られるものです。
デカルバン毛包炎(DF)に加えて、円板状エリテマトーデスは偽毛包の状態にもつながります。活動期には、皮膚病はさまざまなタイプの一次発疹要素によって異なります。DFでは、一次発疹要素は小さな毛包性炎症性丘疹(直径2〜5 mm)であり、その進化は必ずしも毛包性膿疱の形成で終わるわけではありません。中心部では、これらの要素に毛髪が浸透し(時には折れる)、周囲には充血の狭い冠があります。発疹をこすっても激しい痛みはなく、灰色がかった鱗屑と淡黄色の毛包性痂皮は患部表面から簡単に分離されます。病変の中心部では、新しい発疹の形成なしに、脱毛を伴う皮膚の表層萎縮が起こります。DFは、季節に関係なく長く慢性の経過をたどり、日光浴後に増悪がないのが特徴です。病変は孤立性であることが多く、他の部位に病巣はありません。円板状エリテマトーデスの典型的な症例では、発疹の主な要素は炎症性の斑点であり、これが角質増殖を伴うプラークに変化し、萎縮を引き起こします。表面には、角質増殖性の鱗屑がしっかりと付着しており、角質栓が不均一に位置しています。病変をこすると痛みを伴い、鱗屑を表面から剥がすのは困難です。拡大する病変の周囲には充血した縁があり、中心部では毛細血管拡張と脱毛を伴う皮膚萎縮が比較的急速に進行します。皮膚疾患の再発は、皮膚の古い萎縮領域でよく発生します。頭皮に加えて、エリテマトーデスの病変は通常、耳介、鼻梁、頬の頬部などに発生します。これらの皮膚疾患では、病変の組織学的変化も大きく異なります。
毛包性脱毛症(またはルポイド白癬)は、毛包性脱毛症(または毛包性脱毛症)とは異なり、発疹の出現が疾患の活動期にのみ認められる一次発疹要素の出現により異なります。萎縮性脱毛症の病変の縁には、長い経過を経た小さな毛包性炎症性丘疹が見られ、それが単発性の毛包性膿疱へと発展します。これらの皮膚病変による頭皮の損傷は通常は孤立性ですが、まれにルポイド白癬(または毛包性脱毛症)が頬の側頭部や側面にも影響を及ぼすことがあります。毛包性脱毛症(または毛包性脱毛症)では、一次発疹要素は、中央に角質の棘を持つ小さな毛包性の円錐状丘疹であり、萎縮性脱毛症を引き起こします。扁平苔癬の特徴的な病変が、他の皮膚部位(腋窩部や陰部を含む)、口腔粘膜、爪に認められれば、予備診断が容易になります。患部皮膚の組織学的検査によって確定診断することが重要です。これらの皮膚疾患における病理形態学的変化については、既に述べたとおりです。
デカルバン毛包炎(DF、またはループス菌症-LS)の病巣は、発疹の主な要素によって皮膚ループス結核(蛇行性型)とは異なります。頭皮に影響を及ぼすことは稀なループス結核(LT)は、扁平で融合した結節を特徴とし、黄赤色で、柔らかい粘稠度を呈し、透視検査で「リンゴゼリー」のような陽性所見を示します。結節は毛包と関連しておらず、膿疱は形成されません。DF(またはLS)では、毛包性丘疹および単発性膿疱の周囲の病巣の境界領域において、充血がより顕著に現れ、境界が狭くなります。中心領域では、新たな活動性発疹を伴わずに、滑らかで浅い皮膚萎縮と脱毛が見られます。 LTは顔面に限局することが多く、皮膚萎縮を背景に新たな結節(瘢痕の再発)が現れ、潰瘍形成も起こり得ますが、DF(またはLS)ではこのような症状は起こりません。皮膚疾患はそれぞれ異なる組織学的所見を示します。DFは、真皮における毛包内微小膿瘍と毛包周囲の、主にリンパ組織球性の浸潤を特徴とします。LTでは、結核性肉芽腫が真皮に存在し、壊死巣を伴う類上皮細胞の集塊、類上皮細胞間に存在する複数の巨細胞、そして周囲に広がるリンパ細胞の束で構成されています。
頭皮がリーシュマニア症に感染することはほとんどありません。これは、毛髪が蚊の刺咬から身を守ってくれるためです。しかし、生え際に感染が起こる場合があり、晩期潰瘍性(人獣共通性)リーシュマニア症、急性壊死性(人獣共通性)リーシュマニア症、そしてさらに稀ですが、慢性ルポイド(結核性)皮膚リーシュマニア症(LLC)を発症することがあります。いずれの病型でも、瘢痕形成と病変部内での持続的な脱毛が見られます。ルポイド型皮膚リーシュマニア症の症状は、デカルバン毛包炎(またはルポイド白癬)の病変に類似することがあります。これらを鑑別する際には、主要な発疹要素の種類を特定し、既往歴からリーシュマニア症の流行地域に居住していたかどうか、また過去に皮膚リーシュマニア症に罹患していたかどうかを確認する必要があります。DF (LS) とは異なり、LLK は毛包とは関連がなく、瘢痕または瘢痕化したリーシュマニオーマの周囲に現れる黄褐色の小さな結節を特徴とします。結節は通常顔面に限局し、大きさ、色、硬さ、そして陽性の「リンゴゼリー」症状は、扁平型皮膚ループス結核の臨床症状と完全に一致します。したがって、DF (LS) は、その他の点ではループス結核と同様に、皮膚ルポイドリーシュマニア症と鑑別されます。組織学的検査ではLLK病巣に肉芽腫が認められますが、この稀な病態では病原体量が少ないため診断が困難です。結核組織の擦過片から作製した薄層塗抹標本をギムザ・ロマノフスキー法で染色し、繰り返し細菌鏡検を行うことで、LLK病巣におけるリーシュマニア症を検出できます。
デカルバン毛包炎(DF)は、主な発疹要素とその異なる発達によって、頭皮の蛇行性結核性梅毒(BS)とは異なります。DFでは、病変の周辺部に、小さな(2〜5 mm)炎症性毛包性丘疹と個々の毛包性膿疱、鱗屑、痂皮が見られます。結核性蛇行性梅毒では、病変の周辺部に、レンズ豆大の結核が見られ、色は暗赤色で、滑らかで、半球形で、密集しており、毛包とは関連がありません。病変の縁に沿って、それらは密接に集まって融合し、その一部は潰瘍化し、隆起したような急峻な縁、油っぽい底、または表面に血の痂皮のある円形および楕円形の潰瘍を形成します。このような症状は、梅毒瘢痕形成術(DF)(またはLS)では見られず、梅毒瘢痕形成術後に残る、連続性で不均一な細胞萎縮性瘢痕(輪郭は波状で、周辺部には色素沈着を伴う)も同様です。病変の病理形態学的変化も異なります。結核性梅毒では、DFとは対照的に、真皮に肉芽腫性浸潤が認められます。
頭皮のびらん性膿疱性皮膚症は、原因不明の非常にまれな疾患で、近年高齢女性で報告されています。この皮膚疾患は長期にわたる慢性再発性疾患であり、偽性脱毛症(pseudopelad)に至ることもあります。しかし、EPDとDFの臨床症状は異なります。EPDでは、毛包に関連しない扁平膿疱、びらん性潰瘍性皮膚欠損、そして化膿性血性痂皮が頭皮に現れます。DFまたはLSは、思春期以降の男女両方に発症することを考慮する必要があります。これらの皮膚疾患の病理形態学的所見も異なります。 DFの特徴である毛包内微小膿瘍と真皮における毛包周囲および血管周囲のリンパ組織球浸潤とは対照的に、EGでは真皮における非特異的炎症が、表皮およびその付属器の壊死、棘細胞腫、角膜下膿疱を伴う。真皮浸潤では形質細胞が優位であり、初期には白血球破砕性血管炎の徴候が認められる。しかしながら、直接蛍光抗体法は通常陰性である。
デカルバン毛包炎患者の治療
デカルバン毛包炎(またはルポイド性白癬)が疑われる患者は、診断を確定するために(患部皮膚の生検を含む)、また抵抗力低下の具体的な病因(慢性感染巣、代償不全糖尿病、慢性腎炎、異常蛋白血症など)を特定するために、詳細な検査を受ける必要があります。この皮膚疾患の患者に対する全身治療および外用療法は、基本的にブドウ球菌性白癬の治療とほとんど変わりません。抗生物質は、患者の耐性と細菌叢の感受性を考慮しながら、全身的に処方されます。外用には、防腐・殺菌作用のある抗菌剤が使用されます。0.1%グルコン酸クロルヘキシジン溶液、ジオキシジン溶液、0.01%ミラミスチン溶液、フコルチン溶液、および軟膏の形で2%ムピロシンまたは10%マフェニドなどが用いられます。病変の活動性周辺領域では、影響を受けた毛包から毛が除去されます。これらの薬剤が十分に効果を発揮しない場合は、スプレー、ローション、またはクリームの形で、抗生物質とグルココルチコステロイドの併用療法を処方することが推奨されます。治療は増悪期に患者に処方され、長期間、コースで、薬剤を変更しながら実施されます。現在では、病変にX線治療が処方されることはほとんどありません。これは以前は良好な治療効果がありましたが、必ずしも長期的な治療効果があったわけではありません。病変のパターンコピーを動的に比較することで、病気の進行を適時に判断し、合理的な治療法を選択することができます。
偽性ペラデに対する医師の戦術
偽毛包炎の患者を診察する際、主な課題は、局所性萎縮性脱毛症を引き起こした皮膚疾患の病理学的形態を特定することです。まず、偽毛包炎の病態に最も頻繁につながる疾患、例えば萎縮性扁平苔癬、円板状または播種性エリテマトーデス、強皮症、デカルバン毛包炎、萎縮性皮膚真菌症などを除外することが合理的です。診断に至る過程で、医師はいくつかの客観的要因による困難を予想します。そのため、頭皮における皮膚疾患の活動性症状が認められない、または情報提供が困難な場合もあります。これは、疾患の寛解期の始まり、または潜伏期(「くすぶり」)に起因する可能性があります。頭皮の真皮深層部への損傷が主な原因であるため、皮膚表面の炎症性変化はほとんど目立ちません。したがって、この部位における様々な萎縮性皮膚疾患の特徴的な症状は緩和され、臨床的差異が減少します。最も一般的かつ顕著な発疹は、脱毛を伴う局所的な皮膚萎縮です。これは、特に頭皮に限局する場合、偽毛様体の発生につながった皮膚疾患の診断を客観的に複雑化させます。
診断を確定するには、病歴、頭皮だけでなく皮膚表面の残りの部分、毛髪、爪、目に見える粘膜の客観的検査、臨床検査(主に真菌学的および組織学的)が必要です。病歴データに基づいて、局所萎縮性脱毛症に気付いたときの患者の年齢が判明します。したがって、出生時から頭皮に皮膚欠陥があり、将来的に進行が見られない場合は、発達欠陥である先天性皮膚無形成症が疑われます。遺伝性皮膚疾患の中には、小児によく見られるものがあり、偽脱毛症(例えば、先天性および尋常性魚鱗癬、先天性水疱性ジストロフィー性表皮剥離症、色素失調症(女児)、またはジーメンス毛包性角化症(男児)など)につながることがあります。
影響を受けた頭皮を検査する際は、萎縮性脱毛症の病巣に隣接する領域と、偽毛状部に残っている毛束に特に注意を払います。病気の活動期には、これらの領域に典型的な一次発疹要素と二次発疹が見られます。医師は、一次発疹要素と二次発疹要素の形態とその特徴(色、大きさ、形、毛包とのつながり、中央の角質棘の存在、毛髪の変化の可能性など)を一貫して確認する必要があります。一次発疹要素を検出できない場合は、一次要素の進化の結果である二次発疹(びらんまたは潰瘍、痂皮 - 化膿性、血性、漿液性または壊死性など)を検査することが重要です。これは一次要素の特定に間接的に役立ちます。発疹の主要素の種類を考慮して、同じまたは類似の発疹を呈する皮膚疾患の間で鑑別診断が行われます(偽性皮疹状態につながる皮膚疾患の診断アルゴリズムを参照)。
偽毛皮領域の客観的検査を終え、初期の皮膚疾患の発生に関する予備的な見解を形成した後、医師は患者の徹底的な診察に進みます。皮膚表面全体、皮膚付属器および可視粘膜の状態を検査します。頭皮以外の部位に発疹が検出された場合は、その形態学および病理学を一貫して確立します。頭皮以外では、萎縮性皮膚疾患は特徴的な臨床所見を維持します。これは、皮膚の病理形態学的変化にも同様に当てはまります。臨床症状に応じて、必要な臨床検査(真菌学的、細菌学的、組織学的、免疫学的など)を実施します。
ほとんどの場合、偽ペラデ状態と他の部位の皮膚病変は、同じ皮膚疾患によって引き起こされます。したがって、滑らかな皮膚(または粘膜)の発疹の形態と病理学を明らかにすることで、偽ペラデの原因となった基礎疾患の診断をほぼ確実に決定できます。進行性偽ペラデの各症例では、臨床像のみに基づいて信頼性の高い診断を下すことは非現実的であるため、患部の皮膚の組織学的検査が必要です。発疹の特徴的な主要要素がある領域で皮膚生検を行うことをお勧めします。主要な発疹要素の病理形態学的構造に関する結論は、診断を検証する上で重要かつ決定的な要素となります。


